
化学与科学、技术、社会、环境密切相关。下列有关说法中正确的是
A.糖类、蛋白质、油脂都属于天然高分子化合物
B.煤经气化、液化和干馏三个物理变化过程,可变为清洁能源
C.乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的
D.使用含有氯化钠的融雪剂会加快桥梁的腐蚀
科目:高中化学 来源: 题型:
天然存在的金属钫(Fr)极微量。已知其21个同位素都有放射性。它是碱金属元素中最重
的元素。根据它在周期表中的位置预言其性质,其中不正确的是 ( )
A.在已知元素中具有最大的原子半径 B.在空气中燃烧时生成氧化物Fr2O
C.氧化物对应的水化物是极强的碱 D.其单质的熔点比金属钠的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
1862年,比利时化学家索尔维发明了氨碱法制碱,1926年,我国化学家侯德榜创立了
更为进侯德榜制碱法,也叫联合制碱法,两种制碱的生产流程可简要表示如下图:


氨碱法生产流程 联合制碱法生产流程
(1)向沉淀池中通入CO2和氨气时,应先通入氨气的原因是
(2)沉淀池中发生反应的化学反应方程式是 从沉淀池中分离沉淀的操作是
(3)氨碱法生产流程示意图中的Y是 ,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为 .
(4)联合制碱法中从滤液中提取氯化铵晶体的过程推测,所得结论正确是 (选填编号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
d.通入氨气能使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(5)联合制碱法相比于氨碱法,氯化钠利用率从70%提高到90%以上,主要是设计了循环Ⅰ,联合制碱法的另一项优点是
(6)产品纯碱中含有碳酸氢钠,可以用加热分解的方法测定产品中纯碱的质量分数,已知样品质量为ag,加热至质量不再改变时称重为bg,则纯碱的质量分数为
查看答案和解析>>
科目:高中化学 来源: 题型:
影片《阿凡达》中出现了一艘开往潘多拉星球的宇宙飞船。下图是元素周期表中的一部分,表中所列字母分别表示一种元素(选项中的物质都是由下图中的元素组成)。根据以上信息,下列说法正确的是( )
A.e和f组成的化合物可吸收宇航员在宇宙飞船活动舱内产生的由d和f组成的气体
B.活动舱内还要营造一种适合宇航员生存的人工生态环境,即充入a和f的常见单质
C.c和f以原子个数之比为1∶1组成的化合物可用作宇航员所需f单质的来源
D.若潘多拉星球上存在b原子, 但比地球上此元素原子少一个质子

查看答案和解析>>
科目:高中化学 来源: 题型:
已知: 在水溶液中水解的热化学方程式为:
在水溶液中水解的热化学方程式为:

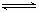

 H=+a
H=+a  ;稀盐酸和稀NaOH的中和热为b
;稀盐酸和稀NaOH的中和热为b  。则等物质的量的
。则等物质的量的 与稀盐酸反应的
与稀盐酸反应的 H等于( )
H等于( )
A.+(a+b)  B.+(a-b)
B.+(a-b) 
C.-(a-b)  D.-(a+b )
D.-(a+b ) 
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.0.1 mol/L氨水中,c(OH-)=c(NH4+)
B.体积和物质的量浓度均相同的稀H2SO4与NaOH溶液充分混合后溶液的pH=7
C.在0.1mol/L CH3COONa溶液中:c(OH-)=c(CH3COOH)+c(H+)
D.0.1mol/L某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关有机物性质的说法正确的是
A.蛋白质可以与酸、碱或重金属盐反应
B.芳香烃都不能使酸性KMnO4溶液褪色
C.CH3CH2OH与氢溴酸不能反应
D.石油的分馏可获得乙烯、丙烯等不饱和烃
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
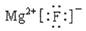
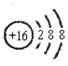
A.硫离子的结构示意图: B.氟化镁的电子式:
C.甘氨酸的结构式:C2H5O2N
D.氢氧化钡的电离方程式:Ba(OH)2=Ba2++(OH)22-
查看答案和解析>>
科目:高中化学 来源: 题型:
如表是ⅥA族部分元素的相关性质。
| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请回答下列问题:
(1)硒的熔点范围可能是 。
(2)碲的化合价可能有 。
(3)硫、硒最高价氧化物对应水化物的酸性强弱顺序是
(填化学式)。
(4)氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中易变质,其可能
发生反应的化学方程式为 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式。
Al2Te3+( )===2Al(OH)3↓+____H2Te↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com