
【题目】下表是元素周期表短周期的一部分:

(1)①表示的元素名称是_________②对应简单离子结构示意图_______。
(2)③位于元素周期表中第________周期,第__________族。
(3)④的单质与 NaOH 溶液反应的离子方程式____________。
(4)⑤在自然界中有质量数为35和37的两种核素,该元素的相对原子质量为35.5,则两核素在自然界中的原子个数之比约为_______。
【答案】碳 ![]() 三周期 ⅡA 族 2Al+2OH- +2H2O=2AlO2-+3H2↑ 3:1
三周期 ⅡA 族 2Al+2OH- +2H2O=2AlO2-+3H2↑ 3:1
【解析】
根据元素周期表的结构可知:①为C元素,②为O元素,③为Mg元素,④为Al元素,⑤为Cl元素,据此答题。
由分析可知:①为C元素,②为O元素,③为Mg元素,④为Al元素,⑤为Cl元素。
(1)①为C元素,其元素名称为碳,②为O元素,其对应简单离子结构示意图为![]() ,故答案为:碳,
,故答案为:碳,![]() 。
。
(2)③为Mg元素,原子序数为12,有3个电子层,最外层有2个电子,所以位于元素周期表的第3周期第ⅡA族,故答案为:三周期,ⅡA族。
(3)④为Al元素,Al与NaOH溶液反应生成偏铝酸钠和氢气,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑。
(4)⑤为Cl元素,氯元素在自然界中有质量数为35和37的两种核素,设其物质的量分别为x、y,该元素的相对原子质量为35.5,则![]()
![]() =35.5,则x:y=3:1,物质的量之比等于其个数之比,所以其原子个数之比约为3:1,故答案为:3:1。
=35.5,则x:y=3:1,物质的量之比等于其个数之比,所以其原子个数之比约为3:1,故答案为:3:1。


科目:高中化学 来源: 题型:
【题目】下图所示是晶体结构中具有代表性的最小重复单元(晶胞)的排列方式,其对应的化学式正确的是(图中:O-X,●-Y,⊕-Z。C选项中Y原子在面上。)( )
A. X2Y B. XY3
B. XY3 C. XY3Z
C. XY3Z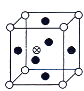 D. XYZ
D. XYZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应。
①用铝与软锰矿(主要成分为MnO2)冶炼锰的原理是________________(用化学方程式来表示)。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是____________________。
③某温度下将氯气通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为1:1,则氯气与KOH反应时,被还原的氯元素和被氧化的氯元素的质量之比为___________。
④12mL 0.lmol/L Na2SO3溶液恰好与4mL 0.lmol/L K2Cr2O7溶液反应,则元素Cr在还原产物中的化合价为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列粒子的空间构型
(1)CO2:_______________________
(2)H2S:____________
(3)SO2:___________
(4)NH4+:_________________
(5)CO32-:_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化铁与氯化亚铁的混合物,现要测定其中铁元素的质量分数,实验按以下步骤进行:

Ⅰ.请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、________(填仪器名称)。
(2)请写出加入溴水发生的离子反应方程式:_______________________________________。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3 g,则接下来还应进行的操作是______________________________。若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
Ⅱ.有同学提出,还可以采用以下方法来测定:

(4)溶解样品改用了硫酸,而不再用盐酸,为什么? ______________________________。
(5)选择的还原剂是否能用铁________(填“是”或“否”),原因是:___________________。
(6)若滴定用掉cmol·L-1KMnO4溶液bmL,则样品中铁元素的质量分数是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:

已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A 的化学名称为__________________,。
(2)B的结构简式为____________________。其核磁共振氢谱显示为______组峰,峰面积比为_______。
(3)由C生成D的反应类型为_____________。
(4)由D生成E的化学方程式为__________________________________________________________。
(5)G中的官能团有__________、__________、__________。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有___________种。(不含立体结构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解法制备硼酸[H3BO3或B(OH) 3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的是( )
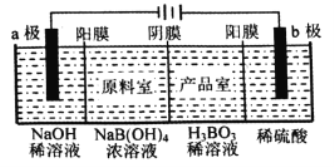
A. 阴极与阳极产生的气体体积比为1:2 B. b极的电极反应式为2H2O-2eˉ=O2↑+4H+
C. 产品室中发生的反应是B(OH)3+OHˉ=B(OH)4ˉ D. 每增加1 mol H3BO3产品,NaOH溶液增重22g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碳酸钠和碳酸氢钠的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为5:4,该混合物中碳酸钠和碳酸氢钠的物质的量之比为
A.1:3B.2:3C.3:4D.4:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com