
| A. | 2s末A和B的转化率相同 | |
| B. | 2s末A的浓度为0.6mol/L | |
| C. | 反应速率$\frac{{v}_{(A)}}{{v}_{(B)}}$=$\frac{1}{2}$ | |
| D. | 用B表示的平均反应速率为0.3mol/(L•s) |
分析 A、将4mol A气体和2molB两种气体混合于固定容积为2L的密闭容器中,反应比和起始量之比相同,所以反应过程中A和B的转化率相同;
B、经2s后测得C的浓度为0.9mol•L-1,所以C的物质的量为1.8mol,所以2s后A的物质的量变化量为:$\frac{1.8mol}{3}×2$=1.2mol,根据c=$\frac{△c}{△t}$计算;
C、速率之比等于对应物质的化学计量数之比;
D、根据c=$\frac{△c}{△t}$计算.
解答 解:A、将4mol A气体和2molB 两种气体混合于固定容积为2L的密闭容器中,反应比和起始量之比相同,所以反应过程中A和B的转化率之比为1:1,故A正确;
B、经2s后测得C的浓度为0.9mol•L-1,所以C的物质的量为1.8mol,所以2s后A的物质的量变化量为:$\frac{1.8mol}{3}×2$=1.2mol,所以2s末A的浓度为$\frac{4mol-1.2mol}{2L}$=1.4mol/L,故B错误;
C、速率之比等于对应物质的化学计量数之比,所以反应速率$\frac{{v}_{(A)}}{{v}_{(B)}}$=$\frac{2}{1}$,故C错误;
D、根据c=$\frac{△c}{△t}$=$\frac{\frac{0.6}{2}mol/L}{2s}$=0.15mol/(L•s),故D错误;
故选A.
点评 本题考查化学平衡计算及影响因素等知识,题目难度中等,试题培养了学生的分析、理解能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | H2SO4═2H++SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | KClO3═K++Cl-+3O2- | D. | NaHSO4═Na++HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
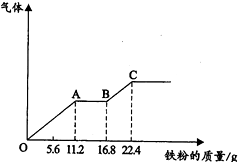 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁质量增加的变化如图所示.反应前后溶液体积不发生变化.
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁质量增加的变化如图所示.反应前后溶液体积不发生变化.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
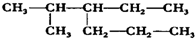
| A. | 2-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-乙基己烷 | D. | 5-甲基-4-乙基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应,只要化学反应的速率很快,理论上都能设计成原电池 | |
| B. | 中和反应一定是放热反应 | |
| C. | 化学反应的速率可通过改变条件而改变 | |
| D. | 化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
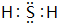 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com