
【题目】研究表明,![]() 可以衰变为
可以衰变为![]() ,则可用来比较这两种元素金属性强弱的方法是( )
,则可用来比较这两种元素金属性强弱的方法是( )
A.比较这两种元素的单质的熔点
B.向氯化铝和氯化镁的溶液中分别滴加过量的氨水
C.将打磨过的镁带和铝片分别与试管中的热水作用,并滴入酚酞溶液
D.将打磨过的铝片和镁带分别投入氢氧化钠溶液中,Al能与![]() 溶液反应放出氢气,而Mg不能
溶液反应放出氢气,而Mg不能
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.甲烷分子(CH4)失去一个H+,形成甲基阴离子(CH3-),变化过程中微粒的键角发生了改变,但碳原子的杂化类型没有改变
B.冰与干冰都是分子晶体,其晶胞中分子的空间排列方式类似
C.因为H2SO3和H2CO3的非羟基氧原子不同,所以它们的酸性不同
D.乳酸[CH3CH(OH)COOH]分子中有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚碳酸酯(简称PC)是重要的工程塑料,某种PC塑料(N)的合成路线如下:
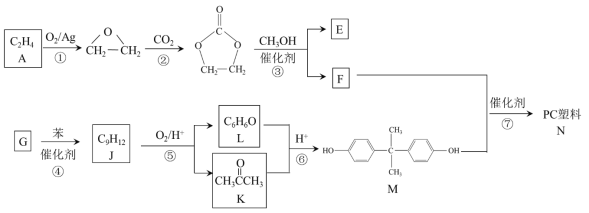
已知:R1COOR2 + R3OH![]() R1COOR3 + R2OH
R1COOR3 + R2OH
(1)①的反应类型是_______________。 K中含有的官能团名称是_______________。
(2)E的名称是_______________。
(3)④是加成反应,G的核磁共振氢谱有三种峰,G的结构简式是__________________。
(4)⑦的化学方程式是______________________________________________。
(5)⑥中还有可能生成分子式为C9H12O2产物。分子式为C9H12O2且符合下列条件的同分异构体共有__________ 种。写出其中两种核磁共振氢谱有5组峰的物质的结构简式_______________________________
a.属于芳香化合物 ,且苯环上只有两个取代基 b.1mol该物质能消耗1molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对一种废旧合金(含有Cu、Fe、Si等元素)进行分离、回收再利用,所设计工艺流程如图。
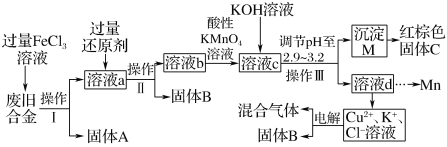
已知:298K时,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Mn(OH)2]=1.9×10-13
回答下列问题:
(1)操作Ⅰ、Ⅱ、Ⅲ为__,固体B为__(填化学式)。
(2)加入过量FeCl3溶液过程中与较不活泼的金属反应的离子方程式__。
(3)调节pH至2.9~3.2的目的是分离__(填离子符号)
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为__。
②若用amol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液VmL,所得红棕色固体C的物质的量为__(用含a、V的代数式表示)
(5)用惰性电极电解时阳极产生标准状况下的气体6.72L,阴极得到的电子数为0.8NA,则生成氧气的物质的量为__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像正确的是( )
A.向CaIOH)2和NaOH的混合溶液中通入CO2 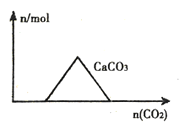
B.向1L浓度均为0.1mol/L的NaAlO2、Ba(OH)2的混合溶液中加入0.1mol/L的稀H2SO4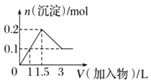
C.向1L浓度分别为0.1mol/L和0.3mol/L的AlCl3、NH4Cl的混合溶液中加入0.1mol/L的稀NaOH溶液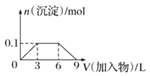
D.向氢氧化钠溶液中滴加明矾溶液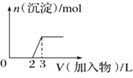
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关节炎病因是在关节滑液中形成尿酸钠晶体,尤其在寒冷季节诱发关节疼痛,其化学历程为:
①HUr(尿酸)+H2O![]() Ur-(尿酸根离子)+H3O+;
Ur-(尿酸根离子)+H3O+;
②Ur-(aq)+Na+(aq)![]() NaUr(s)37℃时Ksp(NaUr)=6.4×10-6
NaUr(s)37℃时Ksp(NaUr)=6.4×10-6
下列叙述中错误的是
A.反应的ΔH<0B.减少食盐的摄入,缓解疼痛症状
C.Ksp(NaUr)随着温度的降低而降低D.升高温度,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象、解释和结论都正确的是
选项 | 实验操作 | 实验现象 | 解释或结论 |
A | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 |
B | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
C | 常温下,用pH计分别测定0.1moI/LNaA溶液的0.1moI/LNaB溶液的pH | pH:NaA>NaB | 能证明酸性:HA>HB |
D | 向盛有1mL0.lmol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1mol/L的NaI溶液,再振荡, | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中,有关微粒的物质的量浓度关系不正确的是
A.0.1mol/L的NaA溶液和0.1mol/L的HA溶液等体积混合pH=4.75,则溶液:c(HA)+c(H+)=c(OH-)+c(A-)
B.0.1mol·L-1(NH4)2Fe(SO4)2溶液:c(NH4+)+2c(Fe2+)+c(H+)=2c(SO42-)+c(OH-)
C.分别用pH=2和pH=3的CH3COOH溶液中和含等物质的量NaOH的溶液,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va<Vb
D.等物质的量浓度的①NH4Cl溶液②(NH4)2SO4溶液③NH4HSO4溶液④(NH4)2CO3溶液⑤NH4HCO3中NH4+浓度的大小关系是②>④>③>①>⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
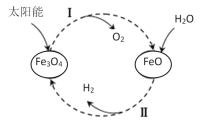
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com