
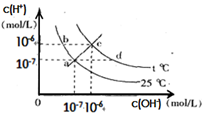
| A. | c点对应的溶液中大量存在的离子可能为:Na+、H+、Cl-、NO3- | |
| B. | 将25℃时的KCl溶液加热到t℃,则该溶液中的c(OH-)由a点变化到b点 | |
| C. | t℃<25℃ | |
| D. | ac线上的任意一点溶液均有c(H+)=c(OH-) |
分析 A.c点溶液中c(H+)=c(OH-),溶液呈中性;
B.KCl溶液呈中性,升高温度增大水的电离,但溶液仍然呈中性;
C.水的电离是吸热反应,升高温度促进水电离,水的离子积常数增大;
D.ac线上任一点都呈中性.
解答 解:A.c点溶液中c(H+)=c(OH-),溶液呈中性,如果溶液中存在Na+、H+、Cl-、NO3-,则该溶液呈酸性,不符合,故A错误;
B.KCl溶液呈中性,升高温度增大水的电离,但溶液仍然呈中性,a点溶液呈中性,但b点c(H+)>c(OH-),故B错误;
C.水的电离是吸热反应,升高温度促进水电离,水的离子积常数增大,根据图知,a点离子积常数小于c,所以t℃>25℃,故C错误;
D.ac线上任一点都呈中性,所以都存在c(H+)=c(OH-),故D正确;
故选D.
点评 本题考查离子积常数及图象分析,为高频考点,侧重考查学生分析判断能力,正确判断各点溶液酸碱性及离子积常数影响因素是解本题关键,易错选项是B.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖(C12H22O11) | 25.00 | 342 |
| 硫酸钾 | 0.84 | 174 |
| 阿司匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| B. | 日常生活中无水乙醇常用于杀菌消毒 | |
| C. | SO2具有漂白性,能使碘的淀粉溶液由蓝色变为无色 | |
| D. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 加入催化剂,有利于合成氨的反应 | |
| C. | 将混合气体中的氨液化,有利于合成氨的反应 | |
| D. | 工业生产硫酸的过程中,使用过量的空气以提高二氧化硫的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com