
| A. | x+y>3 | |
| B. | 反应速率加快,活化分子百分数增加 | |
| C. | A的转化率减小,体积分数增大 | |
| D. | 平衡正向移动,平衡常数增大 |
分析 平衡时测得A的浓度为0.6mol?L-1,保持温度不变,将容器的容积缩小到原来的一半,如平衡不移动,则A的浓度应为1.2mol/L,而此时为1mol/L,则说明增大压强平衡向正方向移动,以此进行判断.
解答 解:平衡时测得A的浓度为0.6mol?L-1,保持温度不变,将容器的容积缩小到原来的一半,如平衡不移动,则A的浓度应为1.2mol/L,而此时为1mol/L,则说明增大压强平衡向正方向移动,
A、增大压强平衡向正方向移动,说明反应物气体的计量数之和大于生成物气体的计量数,应为x+y>3,故A正确;
B、增大压强,单位体积化活分子数增加,而百分数不变,故B错误;
C、增大压强平衡向正方向移动,说明A的转化率增大,体积分数减少,故C错误;
D、平衡常数是温度的函数,温度不变、平衡常数不变,故D错误;
故选A.
点评 本题考查化学平衡移动知识,题目难度不大,注意从浓度的变化的角度判断平衡移动的方向,结合压强对平衡移动的影响分析.


科目:高中化学 来源: 题型:解答题
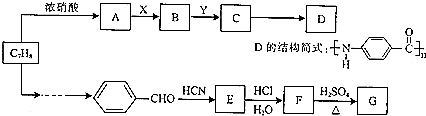
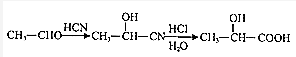
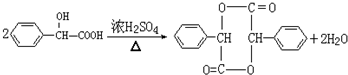 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸是SO2与水反应的产物,显酸性 | |
| B. | SO2溶于水,剧烈反应生成亚硫酸 | |
| C. | 亚硫酸具有漂白性,能够使品红溶液褪色 | |
| D. | 亚硫酸不稳定,容易分解为水和SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 加热蒸干TiCl4溶液 | 产生大量固体 | 固体成分为TiCl4 |
| B | 用双氧水滴定KI淀粉溶液 | 溶液变蓝 | 达到滴定终点 |
| C | 将K3[Fe(CN)6]溶液滴加到某溶液中 | 产生蓝色沉淀 | 该溶液中含有Fe2+ |
| D | 将SO2通入石蕊溶液中 | 溶液褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 ( 25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
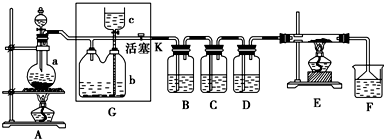
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
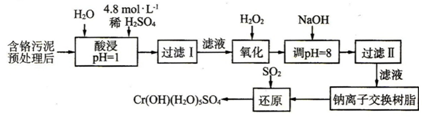
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | ─ | ─ | 4.7 | ─ |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com