
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
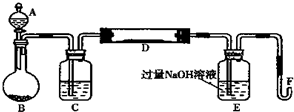
 已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某同学拟用电解硫酸铜溶液的方法测定铜的相对原子质量.该同学向pH=3.8的含有硫酸铁杂质的硫酸铜溶液中加入过量的黑色粉末X,充分搅拌后将滤液用如图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:高一化学(中学生学科素质训练与检测丛书) 题型:013
V mL某硫酸铁溶液中含![]() m g,取
m g,取![]() mL此溶液,稀释成3V mL,那么稀释后溶液中
mL此溶液,稀释成3V mL,那么稀释后溶液中![]() 的物质的量浓度为
的物质的量浓度为
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com