
【题目】化学在环境保护中起着十分重要的作用,电化学降解![]() 的原理如图所示。下列说法不正确的是
的原理如图所示。下列说法不正确的是

A.A为电源的正极
B.溶液中H+从阳极向阴极迁移,阴极区电解质溶液的pH保持不变
C.Ag-Pt电极的电极反应式为![]() +12H++10e-=== N2↑+6H2O
+12H++10e-=== N2↑+6H2O
D.电解过程中,每转移2 mol电子,则左侧溶液质量减少18 g
【答案】B
【解析】
由图示知在![]() 电极上
电极上![]() 发生还原反应,因此
发生还原反应,因此![]() 电极为阴极,则B为负极,A为电源正极;阳极电极反应式:
电极为阴极,则B为负极,A为电源正极;阳极电极反应式:![]() ,阴极电极反应式:
,阴极电极反应式:![]() 。
。
A. 该装置中,硝酸根离子得电子发生还原反应,则![]() 电极为阴极、
电极为阴极、![]() 电极为阳极,连接阴极的B电极为负极,A为正极,故A正确;
电极为阳极,连接阴极的B电极为负极,A为正极,故A正确;
B. 电解时阳离子向阴极移动,阴极电极反应为:![]() ,转移10个电子时,有10个
,转移10个电子时,有10个![]() 由阳极进入阴极,但阴极会消耗12个
由阳极进入阴极,但阴极会消耗12个![]() ,故阴极
,故阴极![]() 减少,PH增大,故B错误;
减少,PH增大,故B错误;
C. 阴极上硝酸根离子得电子发生还原反应,电极反应式为![]() ,故C正确;
,故C正确;
D. 阳极电极反应式为:![]() 转移2mol电子时,阳极消耗1mol水,产生2mol
转移2mol电子时,阳极消耗1mol水,产生2mol![]() (2g)进入阴极室,产生0.5mol(16g)氧气,故阳极室质量减少18g,D正确;
(2g)进入阴极室,产生0.5mol(16g)氧气,故阳极室质量减少18g,D正确;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】TiO2和TiCl4均为重要的工业原料。已知:
Ⅰ.TiCl4(g)+O2(g)![]() TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1
TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1
Ⅱ.2C(s)+O2(g)![]() 2CO(g) ΔH2= -220.9kJ·mol-1
2CO(g) ΔH2= -220.9kJ·mol-1
请回答下列问题:
(1)TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为_____________________。升高温度,对该反应的影响为___________________________________。
(2)若反应Ⅱ的逆反应活化能表示为EkJ·mol-1,则E________220.9(填“>”“<”或“=”)。
(3)t℃时,向10 L恒容密闭容器中充入1molTiCl4和2 molO2,发生反应Ⅰ。5min达到平衡时测得TiO2的物质的量为0.2 mol。
①0~5 min 内,用Cl2表示的反应速率v(Cl2)=__________。
②TiCl4的平衡转化率a=__________________。
③下列措施,既能加快逆反应速率又能增大TiCl4的平衡转化率的是__________(填选项字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分TiO2 D.增大O2浓度
④t℃时,向10 L恒容密闭容器中充入3 mol TiCl4和一定量O2的混合气体,发生反应Ⅰ,两种气体的平衡转化率(a)与起始的物质的量之比(![]() )的关系如图所示:
)的关系如图所示:
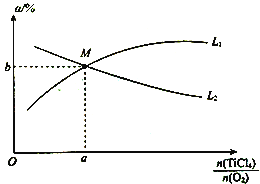
能表示TiCl4平衡转化率的曲线为__________(填“L1”或“L2”);M点的坐标为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
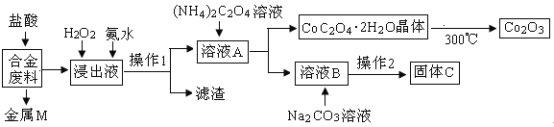
(1)金属M为__________,操作1为___________。
(2)加入H2O2的作用是(用离子方程式表示)________,加入氨水的作用是________。
(3)充分焙烧的化学方程式为____________。
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。操作2中,蒸发浓缩后必须趁热过滤,其原因是___________,90℃时Ksp(Li2CO3)的值为___________。
温度/℃ | 10 | 30 | 60 | 90 |
浓度/molL-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年3月,我国科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法不正确的是
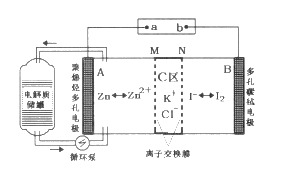
A. 放电时B电极反应式为:I2+2e-=2I-
B. 放电时电解质储罐中离子总浓度增大
C. M为阳离子交换膜,N为阴离子交换膜
D. 充电时,A极增重65g时,C区增加离子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业、硫酸工业的生产工艺流程大致为:
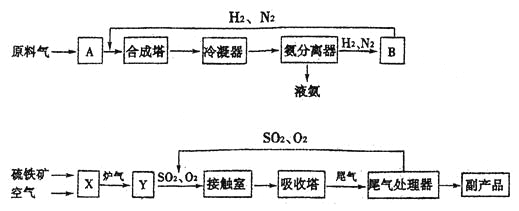
合成塔和接触室中的反应分别为:N2(g)+3H2(g)![]() 2NH3(g) △H﹤0; 2SO2(g)+O2(g)
2NH3(g) △H﹤0; 2SO2(g)+O2(g)![]() 2SO3(g) △H﹤0
2SO3(g) △H﹤0
(1)写出流程中设备的名称:B____________,X___________。
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是_________________。
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是____________(填序号)。
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是_______________________。
(5)工业生产中常用氨——酸法进行尾气脱硫,以达到消除污染、废物利用的目的。硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1B.反应Ⅱ:ΔH>0,T1>T2
C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1D.反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)。各容器中起始物质的量浓度与反应温度如下表所示:
N2(g)+2CO2(g)。各容器中起始物质的量浓度与反应温度如下表所示:
容器 | 温度/℃ | 起始物质的量浓度/(mol·L-1) | |||
NO(g) | CO(g) | N2 | CO2 | ||
甲 | T1 | 0.10 | 0.10 | 0 | 0 |
乙 | T2 | 0 | 0 | 0.10 | 0.20 |
丙 | T2 | 0.10 | 0.10 | 0 | 0 |
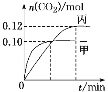
反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示。下列说法正确的是
A.该反应的正反应为放热反应,平衡常数K(T1)<K(T2)
B.乙容器中反应达到平衡时,N2的转化率小于40%
C.达到平衡时,乙容器中的压强一定大于甲容器的2倍
D.丙容器中反应达到平衡后,再充入0.10 mol NO和0.10 mol CO2,此时υ(正)<υ(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用向下排气法在容积为VmL的集气瓶中收集氨气,由于空气尚未排净,最后瓶内气体相对于氢气的密度为9.5,将此盛满气体的集气瓶倒置于水中,瓶内水马上升到一定高度后,即停止上升,则在同温同压下,瓶内剩余气体的体积为
A.![]() VmLB.
VmLB.![]() mLC.
mLC.![]() mLD.无法判断
mLD.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单化合物HB在水中达到电离平衡时各种微粒的浓度如下表所示(25 ℃):分析表中①至⑥的数据,下列说法不正确的是( )

A.①与②的数据都说明化合物HB只有部分电离
B.③与④的数据近似相等,说明HB的电离平衡常数与初始浓度无关
C.⑤与⑥的数据说明加水稀释后HB的电离平衡正向移动
D.⑤与⑥的数据说明起始浓度越大,HB电离的程度越高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com