
| A. | 向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色 | |
| B. | 浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊 | |
| C. | 将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅 |
分析 A.酸性高锰酸钾溶液具有强氧化性,能够氧化草酸;
B.硫代硫酸钠在酸性条件下发生反应生成二氧化硫气体和S单质;
C.压缩后二氧化氮浓度增大,气体颜色变深.
解答 解:A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液,二者发生氧化还原反应导致溶液褪色,故A正确;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合,反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,则混合液变浑浊,故B正确;
C.可逆反应为2NO2?N2O4,将盛有NO2和N2O4混合气体的容器压缩后,平衡向着正向移动,但是由于容器的体积缩小,导致反应后二氧化氮的浓度会增大,则混合气体颜色比压缩前深,故C错误;
故选C.
点评 本题考查了常见元素化合物性质、化学平衡的影响因素等,题目难度中等,明确常见化合物性质为解答关键,注意掌握影响化学平衡的因素,试题培养了学生的分析能力及灵活应用能力.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:选择题

| A. | 滴定过程中总是存在:Ka>Kh | |
| B. | 点②所示溶液中存在:c(Na+)=c(A-) | |
| C. | 点③所示溶液中存在:c(Na+)=c(A-)+c(HA) | |
| D. | 向点①所示溶液中加水:$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$比值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上适应性考试二化学试卷(解析版) 题型:填空题
[化学—选修2:化学与技术]
工业炼铜的方法有由黄铜矿(主要成分是CuFeS2,杂质不含铜元素)炼制精铜的工艺流程示意图如图:
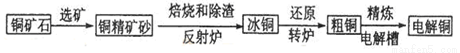
(1).黄铜矿中铜的质量分数为0.4,生产1吨纯铜理论上需要这种黄铜矿____________吨。
(2).在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,_____________________。且部分Fe的硫化物转变为Fe的低价氧化物。
(3).从环保环境和充分利于原料角度看如何处理和利用产生的烟气?___________。
(4).在转炉中,冰铜中的Cu2S先被氧化成Cu2O,,生成的Cu2O再与Cu2S反应,两步反应的热化学方程式为:①2Cu2S(s)+3O2(g)═2Cu2O(s))+2SO2(g)△H=-768.2kJ.mol-1
②2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ.mol-1
则反应Cu2S转化为铜的热化学方程式:_________________________。
将3molCu2S与一定量的空气(氮气、氧气的体积比为4:1)在密闭容器中充分反应(假设各步反应都完全且Cu2S完全参与反应),得到单质铜3mol,所得气体中SO2的体积分数为_____________。
(5).电解精炼铜,电解质溶液为______________,电解一段时间后,电解质溶液的浓度_____________(填“减少”、“不变”、或“增大”)
(6).利于反应Cu+H2O2+H2SO4=CuSO4+2H2O可以制备CuSO4,若将该反应设计为原电池,其正极电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
用如图所示装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是
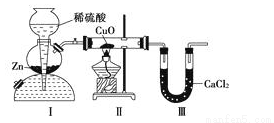
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ 装置中玻璃管内有水冷凝
D.CuO没有全部被还原
查看答案和解析>>
科目:高中化学 来源:2017届山西大学附中高三上10月模块诊断化学试卷(解析版) 题型:选择题
分析生产生活中的下列过程,不涉及氧化还原反应的是( )
A.煤液化制得清洁能源 B .人工固氮
.人工固氮
C.将氯气通入冷的消石灰中制漂白粉 D.从海水中提取氯化镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com