
【题目】在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况)。问:
(1)原溶液中有__________mol Na2CO3,__________mol NaHCO3。
(2)盐酸的物质的量浓度_________。
【答案】0.1 0.3 2.5 mol/L
【解析】
(1)利用n=![]() 计算出CO2的物质的量,利用混合物的质量关系和碳原子守恒来列式计算;
计算出CO2的物质的量,利用混合物的质量关系和碳原子守恒来列式计算;
(2)恰好完全反应,最后生成NaCl,由钠离子的物质的量可知盐酸中HCl的物质的量,再利用c=![]() 计算浓度。
计算浓度。
(1)标准状况下CO2的物质的量为![]() =0.4mol,设Na2CO3和NaHCO3的物质的量分别为x、y,由质量和碳原子守恒可知,106g/mol×x+84 g/mol×y=35.8g,x+y=0.4mol,解得x=0.1 mol,y=0.3 mol,故答案为:0.1;0.3;
=0.4mol,设Na2CO3和NaHCO3的物质的量分别为x、y,由质量和碳原子守恒可知,106g/mol×x+84 g/mol×y=35.8g,x+y=0.4mol,解得x=0.1 mol,y=0.3 mol,故答案为:0.1;0.3;
(2)因恰好完全反应,最后生成NaCl,钠离子的物质的量为0.1mol×2+0.3mol=0.5mol,由NaCl~HCl可知,HCl的物质的量为0.5mol,则盐酸浓度为![]() =2.5 mol/L,故答案为:2.5 mol/L。
=2.5 mol/L,故答案为:2.5 mol/L。


科目:高中化学 来源: 题型:
【题目】25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是

A. 25℃时H2C2O4的一级电离常数为Ka1=104.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定环境中一定能大量共存的是( )
A. pH=1的无色溶液SO42-、Cu2+、Na+、Cl-
B. 使石蕊试纸变蓝的溶液:Na+、K+、S2-、 CO32-
C. 加入铝粉能产生H2的溶液中: NH4+、Na+、Fe2+、 NO3-
D. 水电离出的c(H+)=1.0× ![]() mol/L的溶液中:K+、Na+、Cl-、 HCO3-
mol/L的溶液中:K+、Na+、Cl-、 HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为 0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol电子,若不考虑溶液体积的变化,下列叙述正确的是( )

A. 产生气体体积①=②
B. 电极上析出固体质量①<②
C. 溶液的pH变化:①减小②增大
D. 电极反应式:①中阳极Cu2++2e-=Cu,②中负极Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)1.01×105Pa、0℃时气态单质Xn的密度为d g/L,则X的相对原子质量为________。
(2)NO和O2可发生反应:2NO+O2=2NO2,现有amolNO和bmolO2充分反应后氮原子与氧原子的个数比为_____。
(3)已知铝的相对原子质量为27,若阿伏加德罗常数取6.02×1023mol-1,则可估算一个铝原子的质量约为________g。
(4)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,那么c g氧气在标准状况下的体积约是______(用含NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵(NH4)2Fe(SO4)2是一种重要的化学试剂。现有甲乙两个化学学习小组做了如下实验
Ⅰ.甲学习小组用图甲所示装置制备硫酸亚铁铵,所用药品有铁屑、稀硫酸、(NH4)2SO4溶液。
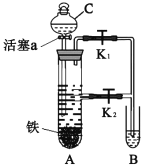
(1)装置C的名称是___________,(NH4)2SO4溶液在___________装置中(填“A”或“B”)。
(2)装置A中发生反应的化学方程式为___________。
(3)将B中的液体倒入蒸发皿蒸干时,往往先加入一定量的硫酸。其作用是在酸性条件下不易被氧化和___________。
(4)为防止B中制得的(NH4)2Fe(SO4)2被氧化变质,实验操作是___________。
Ⅱ.乙学习小组为了探究硫酸亚铁铵分解产物,査阅资料发现:硫酸亚铁铵隔绝空气加热到110℃左右完全分解。气体产物有N2、H2O、NH3和另一气体产物Ⅹ。该学习小组检验X气体的组成。
(5)该学习小组猜想X气体只有三种可能。分别是:i.SO2,ii.SO3,ⅲ.___________。
(6)该小组利用图乙装置进行检验。
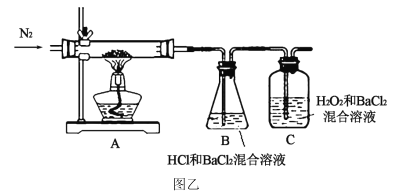
实验现象是B中未出现沉淀,C中溶液变浑浊。得出的结论是___________,C中发生反应的离子方程式是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用NaOH配制0.10molL-1的500mLNaOH溶液的过程如图所示:你认为该同学的错误步骤有( )
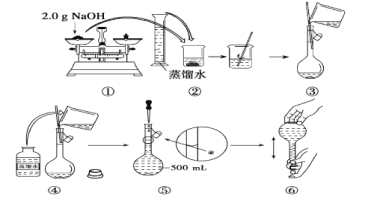
A. 1处B. 2处C. 3处D. 4处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知:四种原了最外层电子数之和为24。下列说法止确的是

A. 元索Ⅹ和元Z的最高正化合价相同
B. 单核阴离子半径的大小顺序为:r(W)>r(X)
C. 气态简单氢化物的热稳定性顺序为:Y<Z<X<W
D. 元素Z的氧化物对应水化物都是强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com