
【题目】严重的雾霾天气的形成与汽车尾气排放有关。汽车尾气中常含有CO、NOx等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处理,设计了下图所示装置(部分夹持装置已略去)。
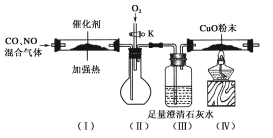
(1)装置(Ⅲ)的主要作用为________________________。
(2)停止加热,打开活塞K,放入适量氧气时,装置(Ⅱ)中可观察到的现象是___________________。
(3)该套装置中有不完善之处,还应在装置(Ⅳ)后补充____________。
(4)工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3===NaNO2+NaNO3+CO2、NO2+NO+Na2CO3===2NaNO2+CO2。现有标准状况下a L NO2和b L NO的混合气体恰好被200 mL Na2CO3溶液完全吸收,则a、b应满足的关系为________。Na2CO3溶液的物质的量浓度为________mol·L-1(不必化简)。
【答案】(1)检验CO是否转化为CO2 (2)出现红棕色气体
(3)尾气处理装置(4)a∶b≥1∶1 ![]()
【解析】(1)CO和NO在催化剂和加热条件下转化为N2和CO2,CO2与澄清石灰水反应生成CaCO3而出现浑浊,所以装置(Ⅲ)的主要作用是检验CO是否转化为CO2。
(2)由于有部分NO没有转化为N2,向装置中通入空气时,装置(Ⅱ)中的NO与O2反应生成红棕色的NO2。
(3)由于尾气中仍残留未反应的CO、NO,所以该套装置应增加尾气处理装置。
(4)根据反应2NO2+Na2CO3===NaNO2+NaNO3+CO2、NO2+NO+Na2CO3===2NaNO2+CO2可知,NO2和NO的物质的量之比应大于或等于1:1,气体才会反应完全。与NO2和NO反应的Na2CO3的物质的量为![]() mol,与NO2单独反应的Na2CO3的物质的量为
mol,与NO2单独反应的Na2CO3的物质的量为![]() mol,故Na2CO3的物质的量浓度为c(Na2CO3)=
mol,故Na2CO3的物质的量浓度为c(Na2CO3)=![]() mol/L。
mol/L。


科目:高中化学 来源: 题型:
【题目】下列有关钠的叙述正确的是( )
①钠在空气中燃烧生成氧化钠
②金属钠可以保存在煤油中
③钠与硫酸铜溶液反应,可以置换出铜
④金属钠有强还原性
⑤钠原子的最外层上只有一个电子,所以在化合物中钠的化合价显+1价
A.①②④B.②③⑤C.①④⑤D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石棉尾矿主要含有Mg3(Si2O5)(OH)4和少量的Fe2O3、Al2O3。以石棉尾矿为镁源制备碳酸镁晶体(MgCO3·nH2O)的工艺如下:
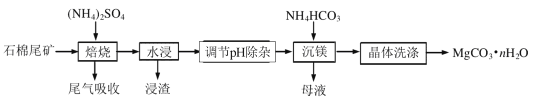
已知“焙烧”过程中的主反应为:
![]()
(1)写出焙烧产物NH3的电子式_____________________。
(2)为提高水浸速率,可采取的措施为_______________________(任写一条),“浸渣”的主要成分为__________________。
(3)“调节pH除杂”时,需将pH调至5.0,则除去的杂质离子是______________,此时溶液中的c(Fe3+)=__________________(已知Ksp[Fe(OH)3]=4.0×10-38)。
(4) “沉镁”过程中反应的离子方程式为_______________________________________。“沉镁”时若温度超过60℃,将产生较多的碱式碳酸镁杂质,原因是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱电解质的电离常数如下表:
弱电解质 | HCOOH | HCN | H2CO3 |
电离常数(25 ℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列说法错误的是( )
A. 结合H+的能力:CO32->CN->HCO3->HCOO-
B. 2CN-+H2O+CO2=2HCN+CO32-
C. 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D. 25 ℃时,反应HCOOH + CN-![]() HCN+ HCOO-的化学平衡常数3.67×105
HCN+ HCOO-的化学平衡常数3.67×105
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A. 往碳酸镁中滴加稀盐酸:CO![]() + 2H
+ 2H![]() = CO2↑+ H2O
= CO2↑+ H2O
B. 用小苏打治疗胃酸过多:HCO![]() + H
+ H![]() = CO2↑+ H2O
= CO2↑+ H2O
C. 盐酸滴入氨水中:H![]() + OH
+ OH![]() = H2O
= H2O
D. 锌溶解于稀硝酸中:Zn+ 2H![]() =Zn2++ H2↑
=Zn2++ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO![]()
![]() (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
(1)A的名称是____,G中含氧官能团的名称是____。
(2)②的反应类型是____,B和F的结构简式分别为______、______。
(3)写出一种能鉴别A和D的试剂:______;C有多种同分异构体,其中属于芳香族化合物的有____种。
(4)写出反应①的化学方程式:_____________。
(5)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选)_________。
为原料设计它的合成路线(其他所需原料自选)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是
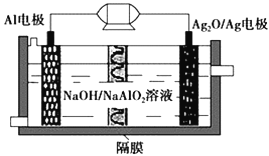
A. 工作时正极发生还原反应,且正极质量逐渐减小
B. 当电极上生成1.08 g Ag时,电路中转移的电子数目为0.1NA
C. Al电极的反应式为Al-3e-+4OH-=AlO2-+2H2O
D. 工作时电解液中的Na+移向Ag2O/Ag电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、Q 是6 种短周期元素,原子序数依次增大。已知X 组成的单质是最理想的气体燃料,Y 是形成化合物种类最多的元素,X 和Z 形成的化合物M 能使酚酞试液变红,W 的原子最外层电子数是次外层电子数的3 倍, R、Q 位于同一周期, R 是该周期中金属性最强的元素,R 与Q 能形成化合物RQ。
请回答下列问题:
(1)Z 在周期表中的位置是_____;
(2)X、Y 形成最简单有机物的分子空间结构是_____;
(3)W 与R 形成的化合物R2W2 可作供氧剂,该化合物含有的化学键类型有_____, 其供氧反应原理是_____(;用化学方程式表示)
(4)在一定条件下,Q 单质能与硫反应生成一种用途广泛的硫化剂S2Q2;S2Q2 与足量水反应有黄色沉淀生成,同时生成能使品红溶液褪色的无色气体,则该反应的化学方程式是_____;
(5)用电子式表示化合物M 的形成过程_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com