
| A. | K+、MnO4-、Ag+、Cl- | B. | Cu2+、NO3-、Na+、OH- | ||
| C. | Fe2+、NH4+、NO3-、SO42- | D. | Al3+、Na+、Cl-、SO42- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=1的酸性溶液中存在大量氢离子,
A.高锰酸根离子为有色离子,银离子与氯离子反应生成难溶物氯化银;
B.铜离子为有色离子,铜离子、氢离子与氢氧根离子反应;
C.亚铁离子为有色离子,酸性条件下硝酸根离子能够氧化亚铁离子;
D.四种离子之间不反应,都是无色离子,都不与氢离子反应.
解答 解:无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=1的酸性溶液中存在大量氢离子,
A.MnO4-为有色离子,Ag+、Cl-之间反应生成氯化银沉淀,在溶液中不能大量共存,故A错误;
B.Cu2+为有色离子,Cu2+、H+与OH-之间发生反应,在溶液中不能大量共存,故B错误;
C.Fe2+为有色离子,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Al3+、Na+、Cl-、SO42-之间不反应,都是无色离子,都不与氢离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA | |
| B. | 1mol/L的氯化铁溶液中,若Cl-的数目为3NA,则Fe3+的数目为NA | |
| C. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,当放出热量9.2 kJ时,转移电子0.6 NA | |
| D. | 标准状况下,11.2L三氯甲烷中含有含极性共价键数目为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
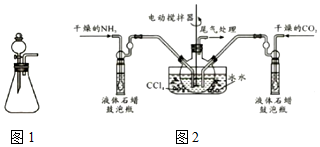
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
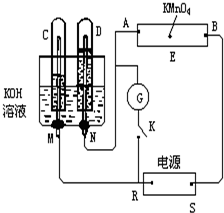 如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.
如图所示,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞.A,B分别为Pt片,压在滤纸两端,R、S为电池的电极.M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极.G为电流计,K为开关.C、D和电解池中都充满浓KOH溶液.若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止试管破裂,加热固体高锰酸钾制氧气时,试管口应略向下倾斜 | |
| B. | 进行SO2性质探究实验时,多余的SO2应排到实验室外 | |
| C. | 为防止药品污染,实验结束后,用剩的白磷可溶解于CS2后倒入垃圾箱 | |
| D. | 配制H2SO4溶液时,先在量筒中加一定体积的水,然后边搅拦边慢慢加入浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥红纸条c不褪色;若关闭活塞b,则c不久褪色.则a溶液(足量)是( )
如图所示,将氯气通入装置.若打开活塞b,则小试管里的干燥红纸条c不褪色;若关闭活塞b,则c不久褪色.则a溶液(足量)是( )| A. | 碳酸钠溶液 | B. | 浓硫酸 | C. | 饱和食盐水 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3和 MgO 的熔点均很高,可用于制作耐高温材料 | |
| B. | 将“地沟油”制成肥皂,可以提高资源的利用率 | |
| C. | 小苏打和氢氧化铝胶囊,可以作内服药治疗胃酸过多 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com