
能量之间可相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
①完成原电池甲的装置示意图(见下图),并作相应标注,要求:在同一烧杯中,电极与溶液含相同的金属元素。
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极__________。
③甲乙两种原电池可更有效地将化学能转化为电能的是________,其原因是____________。
④根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在上述的材料中应选__________作阳极。
通过NOx传感器可监测NOx的含量,其工作原理示意图如下:
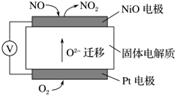
①Pt电极上发生的是________反应(填“氧化”或“还原”)
②写出NiO电极的电极反应式:_________________________________________________。
答案 (1)①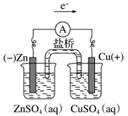 (或其他合理答案)
(或其他合理答案)
②电极逐渐溶解,表面有红色固体析出
③甲 在甲装置中,负极不和Cu2+接触,避免了Cu2+直接与负极发生反应而使化学能转化为热能
④锌片
(2)①还原 ②NO+O2--2e-===NO2
解析 (1)①根据题给条件和原电池的构成条件可得:
a.若用Zn、Cu、CuSO4(aq)、ZnSO4(aq)组成原电池,Zn作负极,Cu作正极,Zn插入到ZnSO4(aq)中,Cu插入到CuSO4(aq)中。
b.若用Fe、Cu、FeSO4(aq)、CuSO4(aq)组成原电池,Fe作负极,Cu作正极,Fe插入到FeSO4(aq)中,Cu插入到CuSO4(aq)中。
c.注意,画图时要注意电极名称,电极材料,电解质溶液名称(或化学式),并形成闭合回路。
②由于金属活动性Zn>Fe>Cu,锌片或铁片作负极,由于Zn或Fe直接与CuSO4溶液接触,工作一段时间后,负极逐渐溶解,表面有红色固体析出。
③带有盐桥的甲原电池中负极没有和CuSO4溶液直接接触,二者不会直接发生置换反应,化学能不会转化为热能,而是几乎全部转化为电能;而原电池乙中的负极与CuSO4溶液直接接触,两者会发生置换反应,部分化学能转化为热能,化学能不可能全部转化为电能。
④由牺牲阳极的阴极保护法可得,铁片作正极(阴极)时被保护,作负极(阳极)时被腐蚀,所以应选择比铁片更活泼的锌作负极(阳极)才能有效地保护铁不被腐蚀。
(2)由图示可知原电池发生反应为2NO+O2===2NO2,NO为还原剂,O2为氧化剂,O2在Pt电极得电子发生还原反应:O2+4e-===2O2-。NO在NiO电极上失电子发生氧化反应:NO+O2--2e-===NO2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO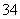 +2I-+2H+??AsO
+2I-+2H+??AsO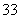 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
下列叙述中正确的是( )
A.甲组操作时,电流表(A)指针不发生偏转
B.甲组操作时,溶液颜色变浅
C.乙组操作时,C2作正极
D.乙组操作时,C1上发生的电极反应为I2+2e-===2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH—Ni电池)。下列有关说法不正确的是( )
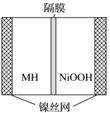
A.放电时正极反应为NiOOH+H2O+e-—→Ni(OH)2+OH-
B.电池的电解液可为KOH溶液
C.充电时负极反应为MH+OH-—→H2O+M+e-
D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高
查看答案和解析>>
科目:高中化学 来源: 题型:
锂空气电池作为新一代大容量电池而备受瞩目,其工作原理如图所示。下列有关锂空气电池的说法不正确的是( )
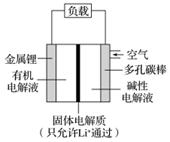
A.随着电极反应的不断进行,正极附近的电解液pH不断升高
B.若把碱性电解液换成固体氧化物电解质,则正极会因为生成Li2O而引起碳孔堵塞,不利于正极空气的吸附
C.放电时,当有22.4 L O2(标准状况下)被还原时,溶液中有4 mol Li+从左槽移动到右槽
D.锂空气电池又称作“锂燃料电池”,其总反应方程式为4Li+O2===2Li2O
查看答案和解析>>
科目:高中化学 来源: 题型:
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。下图是钒电池基本工作原理示意图:
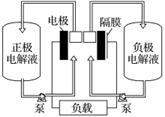
请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是____________,实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是____。
(2)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO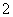 )为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O
)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O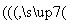 V2++VO
V2++VO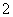 +2H+。放电时的正极反应式为______________________________________________________,充电时的阴极反应式为______________________________________。放电过程中,电解液的pH________(填“升高”、“降低”或“不变”)。
+2H+。放电时的正极反应式为______________________________________________________,充电时的阴极反应式为______________________________________。放电过程中,电解液的pH________(填“升高”、“降低”或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是________(填字母)。
a.VO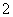 、VO2+混合液 b.V3+、V2+混合液
、VO2+混合液 b.V3+、V2+混合液
c.VO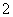 溶液 d.VO2+溶液
溶液 d.VO2+溶液
e.V3+溶液 f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
三个化学小组的同学测定某Na2CO3固体样品(仅含NaOH杂质)的纯度,他们提出了各自的气体分析法。
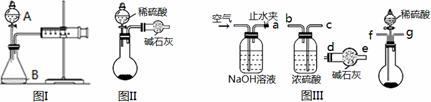
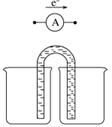
(1)第一小组用图I所示装置,仪器A的名称 。把m1 g的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时需检查该装置气密性,具体的操作方法是 。
(2)第二小组用图II装置测定CO2的质量。该装置存在明显缺陷是:
。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的仪器如图III,装置的连接顺序是a— (填写接口字母,图中仪器可重复使用)。实验中取了样品m1 g,称量干燥管质量为m2 g,与足量稀硫酸反应后称量干燥管质量为m3 g,则Na2CO3的纯度表达式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于25℃的NaHCO3溶液的相关事实,能够证明H2CO3为弱酸的是
A.溶液中存在CO32- B.溶液中c(Na+)>c(CO32-)
C.与等物质的量的NaOH恰好中和 D.溶液中c(H+)·c(OH-)=10-14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com