
ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
A£®1 molH2ÖŹĮæĪŖ2 g
B£®H2OµÄĦ¶ūÖŹĮæĪŖ18 g
C£®±źæöĻĀ44 g CO2µÄĢå»żĪŖ22.4 L
D£®9.8 g H2SO4ŗ¬1molµÄH2SO4·Ö×Ó

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğøŹĖąŹ”ø߶žÉĻѧʌµŚŅ»“Ī¶ĪÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ķ¬Ź±¶ŌÅ©×÷ĪļŹ©ÓĆŗ¬N”¢P”¢KµÄČżÖֻƷŹ£¬¶Ōøų¶ØµÄĻĀĮŠ»Æ·Ź£ŗ¢ŁK2CO3”¢¢ŚKCl”¢¢ŪCa£ØH2PO4)2”¢¢Ü£ØNH4)2SO4£¬¢Ż°±Ė®£¬×īŹŹµ±µÄ×éŗĻŹĒ
A£®¢Ł¢Ū¢Ü B£®¢Ł¢Ū¢Ż C£®¢Ś¢Ū¢Ü D£®¢Ś¢Ū¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗž±±Ź”»ĘŹÆŹŠøßŅ»ÉĻѧʌ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ŗ£ŃóÖ²ĪļČēŗ£“ų”¢ŗ£ŌåÖŠŗ¬ÓŠ·įø»µÄµāŌŖĖŲ£¬Ö÷ŅŖŅŌµā»ÆĪļŠĪŹ½“ęŌŚ”£ÓŠŅ»»ÆѧæĪĶāŠ”×éÓĆŗ£“ųĪŖŌĮĻÖĘȔɣĮæµāµ„ÖŹ£¬ĖūĆĒ½«ŗ£“ų×ĘÉճɻŅ£¬ÓĆĖ®½žÅŻŅ»¶ĪŹ±¼ä(ŅŌČƵā»ÆĪļ³ä·ÖČܽāŌŚĖ®ÖŠ)£¬µĆµ½ŗ£“ų»ŅŠü×ĒŅŗ£¬Č»ŗó°“ŅŌĻĀŹµŃéĮ÷³ĢĢįČ”µ„ÖŹµā£ŗ

£Ø1£©×ĘÉÕŗ£“ųŹ±ŠčŅŖÓƵ½µÄŹµŃéŅĒĘ÷ŹĒ__________________(“ÓĻĀĮŠŅĒĘ÷ÖŠŃ”³öĖłŠčµÄŅĒĘ÷£¬ÓƱźŗÅ×ÖÄøĢīŠ“ŌŚæհד¦)”£
A ÉÕ± B ŪįŪö
C ±ķĆęĆó D ŪįŪöĒÆ
E ¾Ę¾«µĘ F Ĺȿ½Ē G Čż½Å¼Ü
£Ø2£©Öø³öĢįČ”µāµÄ¹ż³ĢÖŠÓŠ¹ŲµÄŹµŃé²Ł×÷Ćū³Ę£ŗ¢Ł___________£¬¢Ū___________”£
£Ø3£©²Ł×÷¢ŪÖŠĖłÓƵÄÓŠ»śŹŌ¼ĮæÉŅŌŹĒ___________(Ö»ĢīŅ»ÖÖ)£¬¼ņŹöŃ”ŌńĘäĄķÓÉ______________”£
£Ø4£©“Óŗ¬ÓŠµāµÄÓŠ»śČܼĮÖŠ»ńČ”µā£¬³£ÓĆĖ®Ō”¼ÓČČÕōĮóµÄ·½·Ø£¬ĘäÓŵćŹĒ_______£¬×īŗó¾§Ģ¬µāŌŚ__________ Ąļ¾Ū¼Æ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØŹ”ø£°²ŹŠø߶žÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø12·Ö£©½šŹōĢśŹĒÓ¦ÓĆ¹ć·ŗ£¬ĢśµÄĀ±»ÆĪļ”¢Ńõ»ÆĪļŅŌ¼°øß¼ŪĢśµÄŗ¬ŃõĖįŃĪ¾łĪŖÖŲŅŖ»ÆŗĻĪļ”£
£Ø1£©ŅŖČ·¶ØĢśµÄijĀČ»ÆĪļFeClxµÄ»ÆѧŹ½£¬æÉĄūÓĆĄė×Ó½»»»ŗĶµĪ¶ØµÄ·½·Ø”£ŹµŃéÖŠ³ĘČ”3.25gµÄFeClxѳʷ£¬ČܽāŗóĻČ½ųŠŠŃōĄė×Ó½»»»Ō¤“¦Ąķ£¬ŌŁĶعżŗ¬ÓŠ±„ŗĶOH-µÄŅõĄė×Ó½»»»Öł£¬Ź¹Cl-ŗĶOH-·¢Éś½»»»”£½»»»Ķź³Éŗó£¬Į÷³öČÜŅŗµÄOH-ÓĆ1.0 mol”¤L-1µÄŃĪĖįÖŠŗĶµĪ¶Ø£¬ÕżŗĆÖŠŗĶŹ±ĻūŗÄŃĪĖį60.0mL”£¼ĘĖćøĆѳʷ֊ĀȵÄĪļÖŹµÄĮ棬²¢Ēó³öFeClxÖŠxµÄÖµ£ŗ
£ØĮŠ³ö¼ĘĖć¹ż³Ģ£©”£
£Ø2£©ĻÖÓŠŅ»ŗ¬ÓŠFeCl2ŗĶFeCl3µÄ»ģŗĻĪļѳʷ£¬²ÉÓĆÉĻŹö·½·Ø²āµĆn(Fe)”Ćn(Cl) = 1”Ć2.8£¬ŌņøĆѳʷ֊FeCl3µÄĪļÖŹµÄĮæ·ÖŹżĪŖ ”£
£Ø3£©°ŃSO2ĘųĢåĶØČėFeCl3ČÜŅŗÖŠ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
£Ø4£©øßĢśĖį¼Ų(K2FeO4)ŹĒŅ»ÖÖĒæŃõ»Æ¼Į£¬æÉ×÷ĪŖĖ®“¦Ąķ¼ĮŗĶøßČŻĮæµē³Ų²ÄĮĻ”£FeCl3ŗĶKClOŌŚĒæ¼īŠŌĢõ¼žĻĀ·“Ó¦æÉÖĘČ”K2FeO4£¬Ęä·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £»ÓėMnO2”ŖZnµē³ŲĄąĖĘ£¬K2FeO4”ŖZnŅ²æÉŅŌ×é³É¼īŠŌµē³Ų£¬ĘäÖŠZn¼«µÄµē¼«·“Ó¦Ź½ĪŖ £¬K2FeO4µÄµē¼«·“Ó¦Ź½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓÄĻŹ”ø߶žÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ£ŗ2H2(g)£«O2(g)£½2H2O(l) ¦¤H£½£571.6 kJ”¤mol£1
2CH3OH(l)£«3O2(g)£½2CO2(g)£«4H2O(l) ¦¤H£½£1452 kJ”¤mol£1
H£«(aq)£«OH£(aq)£½H2O(l) ¦¤H£½£57.3 kJ”¤mol£1
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®H2(g)µÄČ¼ÉÕČČĪŖ571.6 kJ
B£®Ķ¬ÖŹĮæµÄH2(g)ŗĶCH3OH(l)ĶźČ«Č¼ÉÕ£¬H2(g)·Å³öµÄČČĮæ¶ą
C£® H2SO4(aq)£«
H2SO4(aq)£« Ba(OH)2(aq)£½
Ba(OH)2(aq)£½ BaSO4(s)£«H2O(l) ¦¤H£½£57.3 kJ”¤mol£1
BaSO4(s)£«H2O(l) ¦¤H£½£57.3 kJ”¤mol£1
D£®3H2(g)£«CO2(g)£½CH3OH(l)£«H2O(l) ¦¤H£½£«135.9 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”øßŅ»ÉĻѧʌµŚ¶ž“ĪÕļ¶ĻŠŌ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŃõ»Æ»¹Ō·“Ó¦µÄŠšŹöÖŠÕżČ·µÄŹĒ
A£®ÓŠµ„ÖŹ²Ī¼Ó»ņÓŠµ„ÖŹÉś³ÉµÄ·“Ó¦Ņ»¶ØŹĒŃõ»Æ»¹Ō·“Ó¦
B£®Ńõ»Æ»¹ŌµÄ±¾ÖŹŹĒŌŖĖŲ»ÆŗĻ¼ŪµÄÉż½µ
C£®Ź§µē×ӵķ“Ó¦ĪļŌŚ·“Ó¦ÖŠ×÷Ńõ»Æ¼Į£¬·“Ó¦ÖŠ±»»¹Ō
D£®½šŹōµ„ÖŹŌŚ»Æѧ·“Ó¦ÖŠŅ»¶Ø×÷»¹Ō¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗž±±Ź”ŌęŃōŹŠøßČżÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚa L Al2(SO4)3ŗĶ(NH4)2SO4µÄ»ģŗĻČÜŅŗÖŠ¼ÓČėb mol BaCl2£¬Ē”ŗĆŹ¹ČÜŅŗÖŠµÄSO42-ĶźČ«³Įµķ£»Čō¼ÓČė×ćĮæĒæ¼ī²¢¼ÓČČæɵƵ½c mol NH3£¬ŌņŌČÜŅŗÖŠµÄAl3£«ÅضČ(mol/L)ĪŖ
A£® B£®
B£® 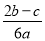 C£®
C£®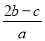 D£®
D£®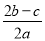
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓÄĻŹ”ø߶žÉĻѧʌµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø12·Ö£©ŅŃÖŖĒ¦Šīµē³ŲµÄ¹¤×÷ŌĄķĪŖPb£«PbO2£«2H2SO4 2PbSO4£«2H2O£¬ĻÖÓĆČēĶ¼×°ÖĆ½ųŠŠµē½ā(µē½āŅŗ×ćĮæ)£¬²āµĆµ± Ē¦Šīµē³ŲÖŠ×ŖŅĘ0.4 molµē×ÓŹ±Ģśµē¼«µÄÖŹĮæ¼õÉŁ11.2 g”£Ēė»Ų“š ĻĀĮŠĪŹĢā”£
2PbSO4£«2H2O£¬ĻÖÓĆČēĶ¼×°ÖĆ½ųŠŠµē½ā(µē½āŅŗ×ćĮæ)£¬²āµĆµ± Ē¦Šīµē³ŲÖŠ×ŖŅĘ0.4 molµē×ÓŹ±Ģśµē¼«µÄÖŹĮæ¼õÉŁ11.2 g”£Ēė»Ų“š ĻĀĮŠĪŹĢā”£
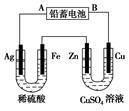
£Ø1£©AŹĒĒ¦Šīµē³ŲµÄ ¼«£¬Ē¦Šīµē³ŲÕż¼«·“Ó¦Ź½ĪŖ £¬·Åµē¹ż³ĢÖŠµē½āŅŗµÄĆÜ¶Č (Ģī”°¼õŠ””±”¢”°Ōö“ó”±»ņ”°²»±ä”±)”£
£Ø2£©Agµē¼«µÄµē¼«·“Ó¦Ź½ŹĒ £¬øƵē¼«µÄµē¼«²śĪļ¹² g”£
£Ø3£©Cuµē¼«µÄµē¼«·“Ó¦Ź½ŹĒ £¬CuSO4ČÜŅŗµÄÅØ¶Č (Ģī”°¼õŠ””±”¢”°Ōö“ó”±»ņ”°²»±ä”±)
£Ø4£©ČēĶ¼±ķŹ¾µē½ā½ųŠŠ¹ż³Ģ֊ijøöĮæ(ׯ×ų±źx)Ėꏱ¼äµÄ±ä»ÆĒśĻߣ¬Ōņx±ķŹ¾ ”£

a£®ø÷UŠĪ¹ÜÖŠ²śÉśµÄĘųĢåµÄĢå»ż
b£®ø÷UŠĪ¹ÜÖŠŃō¼«ÖŹĮæµÄ¼õÉŁĮæ
c£®ø÷UŠĪ¹ÜÖŠŅõ¼«ÖŹĮæµÄŌö¼Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”ø߶žÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚC£Øs£©+CO2£Øg£©?2CO£Øg£©·“Ó¦ÖŠæÉŹ¹·“Ó¦ĖŁĀŹŌö“óµÄ“ėŹ©ŹĒ
¢ŁĖõŠ”ČŻĘ÷µÄĢå»ż£»¢ŚŌö¼ÓĢ¼µÄĮ棻¢ŪĶØČėCO2£»¢ÜŗćŃ¹ĻĀ³äČėN2£»¢ŻŗćČŻĻĀ³äČėN2£»¢ŽĶØČėCO£®
A£®¢Ł¢Ū¢Ż B£®¢Ś¢Ü¢Ž C£®¢Ł¢Ū¢Ž D£®¢Ū¢Ż¢Ž
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com