
| A. | H2SeO3和H2SeO4第一步电离程度大于第二部电离的最主要原因是第一步电离出的氢离子对第二步电离有抑制作用 | |
| B. | 同浓度的H2SeO4的酸性强于硫酸 | |
| C. | H2SeO3和H2SeO4的非羟基氧分别为3和4 | |
| D. | H2SeO4中Se原子的杂化方式为sp3 |
分析 A、第一步电离后生成的负离子,较难再进一步电离出带正电荷的氢离子;
B、硫的非金属性强于Se,所以最高价氧化物对应水化物的酸性硫酸强于H2SeO4;
C、H2SeO3和H2SeO4的非羟基氧分别为1和2;
D、H2SeO4中中心原子Se形成四个Se-Oσ键.
解答 解:A、第一步电离后生成的负离子,较难再进一步电离出带正电荷的氢离子,故H2SeO3和H2SeO4第一步电离程度大于第二步电离,故A错误;
B、硫的非金属性强于Se,所以最高价氧化物对应水化物的酸性硫酸强于H2SeO4,所以硫酸的酸性强,故B错误;
C、H2SeO3和H2SeO4的非羟基氧分别为1和2,故C错误;
D、H2SeO4中中心原子Se形成四个Se-Oσ键,所以Se原子的杂化方式为sp3,故D正确;
故选D.
点评 本题主要考查了弱电解质的电离、酸性强弱的比较、原子杂化方式,难度不大,解题中注意对分子结构的分析.


科目:高中化学 来源: 题型:选择题
| A. | 地沟油经处理后可用作生物柴油 | |
| B. | 金属钠着火可用泡沫灭火器灭火 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 氢氧化铁胶体的分散质粒子不能通过滤纸孔隙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1Na2S溶液中存在;c(OH-)═c(H+)+c(HS-)+2c(H2S) | |
| B. | 常温下,HA溶液与0.1 mol•L-1NaOH溶液正好完全反应时,溶液中一定存在:c(Na+)═c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,向0.1 mol•L-1CH3COOH 溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的10倍 | |
| D. | 常温下,pH=7的CH3COONa和CH3COOH混合溶液中:c(Na+)=0.1 mol•L-1;c(Na+)═c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液中:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)+c(C2O42-) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)=2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2混合溶液:c(Na+)+2c(Ca2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时某物质溶液的pH>7,则该物质一定是碱或强碱弱酸盐 | |
| B. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1<10c2 | |
| C. | 两种amol/LNaX溶液和bmol/LNaY正盐稀溶液,若a>b,测得c(X-)=c(Y-),可推出溶液中的c(HX)>c(HY) | |
| D. | 向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中$\frac{{c(O{H^-})}}{{c(N{H_3}•{H_2}O)}}$增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{2}{5}$mol | B. | $\frac{4}{5}$mol | C. | $\frac{6}{5}$mol | D. | $\frac{22}{5}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 20℃ | K2CO3 | KHCO3 | K2MnO4 | KMnO4 |
| s(g/100g水) | 111 | 33.7 | 11.1 | 6.34 |
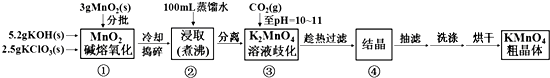
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com