
【题目】硒元素(Se)是第4周期ⅥA族元素,单质有红硒、黑硒和灰硒,灰硒是良好的半导体材料,硒最特殊的性质是在光照射下导电性可提高近千倍,可用于制造光电管。请回答下列问题:
(1)基态Se原子价电子的轨道表示式为__。
(2)As和Se是同一周期元素,As的第一电离能比Se大,原因是___。
(3)硒在空气中燃烧能生成SeO2,常温下,SeO2是易挥发的白色固体,熔点为340~350℃,315℃时升华,则SeO2固体是___晶体;写出一种与SeO2互为等电子体的阴离子的化学式__。
(4)H2SeO4和H2SO4相似,是一种不易挥发的强酸。SeO42-的空间构型为___,中心原子的杂化方式为___。
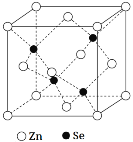
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,Zn原子的配位数为___,若该晶胞密度为ρg·cm-3,硒化锌的摩尔质量为Mg·mol-1,用NA代表阿伏加德罗常数,则晶胞参数a(即晶胞的边长)为___nm。
【答案】![]() As的4p能级是半充满状态,比较稳定 分子 NO2- 正四面体形 sp3杂化 4
As的4p能级是半充满状态,比较稳定 分子 NO2- 正四面体形 sp3杂化 4 ![]() ×107
×107
【解析】
(1)硒为34号元素,有6个价电子, 所以基态Se原子价电子的轨道表示式为![]() 因此,本题正确答案是:
因此,本题正确答案是: ![]() ;
;
(2)同一周期中,元素的第一电离能随着原子序数增大而呈增大趋势,但第ⅤA族元素的P轨道上是半充满状态,比较稳定,所以第一电离能大于相邻元素, As为第ⅤA族元素,Se为第IVA族元素,所以As的第一电离能比Se大,答案:As的4p能级是半充满状态,比较稳定;
(3) SeO2常温下白色晶体,熔、沸点低,所以属于分子晶体;二氧化硒分子中价层电子对=2+1/2(6-2×2)=3,Se原子的杂化类型为SP2,且含有一个孤电子对, 属于V形;与NO2-的价电子和原子数都相等,属于SeO2的等电子体,所以NO2-与SeO2互为等电子体;因此,本题答案是:分子晶体; NO2-;
(4) SeO42-的中心原子的价层电子对数为(6+2)/2=4,所以Se杂化方式为sp3杂化,离子中没有孤电子对,所以SeO42-的立体构型是正四面体形。
因此,本题答案是: sp3;正四面体形。
(5)根据硒化锌晶胞结构图可以知道,每个锌原子周围有4个硒原子,每个硒原子周围也有4个锌原子,所以硒原子的配位数为4,该晶胞中含有硒原子数为8×1/8+6×1/2=4,含有锌原子数为4,根据ρ=m/V=4M/NAV,所以V=4M/ρNA,则晶胞的边长为![]() cm=
cm=![]() ×1010pm,
×1010pm,
因此,本题正确答案是:4; ![]() ×1010pm
×1010pm


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】科学研究发现,具有高度对称的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为化学界关注的热点。立体烷烃中有一系列对称结构的烃,如:![]() (正四面体烷C4H4)、
(正四面体烷C4H4)、![]() (棱晶烷C6H6)、
(棱晶烷C6H6)、![]() 立方烷C8H8)等,下列有关说法正确的是
立方烷C8H8)等,下列有关说法正确的是
A. 立体烷烃的C原子都形成4个单键,因此它们都属于烷烃
B. 上述一系列物质互为同系物,它们的通式为C2nH2n(n≥2)
C. 棱晶烷与立方烷中碳原子均为饱和碳原子,其二氯代物的种数不同
D. 苯、盆烯(![]() )与棱晶烷属于同分异构体
)与棱晶烷属于同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:KClO3+H2C2O4+H2SO4![]() ClO2↑+K2SO4+CO2↑+H2O(未配平)下列说法正确的是
ClO2↑+K2SO4+CO2↑+H2O(未配平)下列说法正确的是
A.KClO3在反应中得到电子B.ClO2是氧化产物
C.H2C2O4在反应中被还原D.1 mol KClO3参加反应有2 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分。当左边充入2molN2,右边充入CO和CO2的混合气体共18g时,隔板处于如图位置(左、右两侧温度相同)。右侧CO2与CO分子数之比为( )

A.3:1B.1:1C.1:2D.1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合肥市某高中化学非限定性课程学习小组利用铁锈(Fe2O3)做了系列实验,物质之间的关系图如下。
根据所学知识回答以下问题:

IHCl的配制
实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制480mL0.1mol/L的盐酸溶液。
(1)配制480mL0.1mol/L的盐酸溶液需要浓盐酸的体积为___mL。(保留2位有效数字)
(2)除了烧杯、玻璃棒、量筒、胶头滴管和试剂瓶还需要的仪器有___。
(3)若出现如下情况,对所配溶液浓度将有何影响?(填“偏低”或“偏高”)
未洗涤烧杯___;定容时俯视刻线____。
II探究实验
(1)写出由A滴入到沸水中制备B的化学方程式。___
(2)下列说法正确的有___(填序号)。
①B转换成C发生了化学反应
②由A制备B,加热越久越好
③物质B具有丁达尔效应
④把B和C组成的混合物过滤,滤液是无色的
⑤整个过程都不涉及到氧化还原反应
(3)向红褐色沉淀C中加入NaClO和NaOH混合溶液,生成一种高效杀菌净水剂Na2FeO4,已知每生成0.2mol的Na2FeO4消耗0.3molNaClO,则该反应的还原产物为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素是一种天然香料,存在于黑香豆、兰花等植物中。工业上常用水杨醛与乙酸酐在催化剂存在下加热反应制得,反应如下(部分生成物已略去):
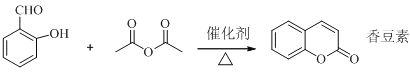
以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去):
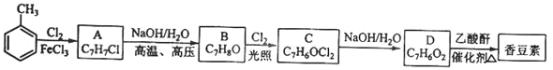
已知:① A中有五种不同化学环境的氢原子;②同一个碳原子上连有两个羟基的结构不稳定,易脱水形成羰基。请回答下列问题:
(1)香豆素的分子式为_______________。
(2)由甲苯生成A的反应类型为____________。A的化学名称为___________。
(3)由B生成C的化学反应方程式为____________________。
(4)B的同分异构体中含有苯环的还有______种,其中在核磁共振氢谱中只出现四组峰的有______种。
(5)D的同分异构体中含有苯环的还有________种,其中属于羧酸类的是_________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取氯气并以氯气为原料进行特定反应的装置。其中:A中盛有MnO2,B中盛有浓盐酸。

(1)用下列两种方法制取氯气:
①用含HCl146g的浓盐酸与足量的MnO2反应;
②用87gMnO2与足量的浓盐酸反应。不考虑HCl的挥发,
则两种方法生成的氯气的量是方法①___②(填“>”、“<”或“=”)。
(2)仪器B的名称是__。
(3)C中盛饱和食盐水(氯气在其中的溶解度很小),是为了除去氯气中混有的__气体。
(4)仪器D用来干燥氯气,其中盛放的试剂是__。
(5)E中装铁粉,其中发生反应的化学方程式是__。
(6)G中盛有NaOH溶液,目的是___。其中发生反应的离子方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲醛和苯酚为主要原料,经下列转化可合成酚醛树脂和重要的有机合成中间体D(部分反应条件和产物已略去)
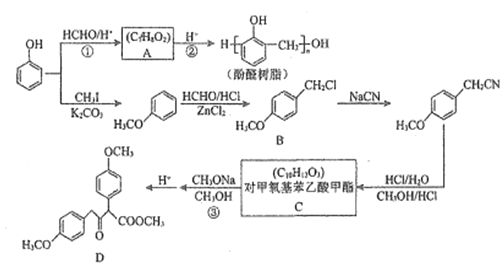
已知:R1CH2COOCH2+R2COOCH3![]() CH3OH+
CH3OH+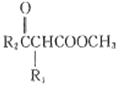
请回答下列问题:
(1)反应①的反应类型为___________;A的化学名称为___________。
(2)C中所含官能团的名称为___________;D的分子式为___________。
(3)反应②的化学方程式为______________________。
(4)A的下列性质中,能反映支链对苯环结构产生影响的是___________(填字母)。
a.能与氢氧化钠溶液反应
b.能使酸性高锰酸钾溶液褪色
c.向稀溶液中加入浓溴水后,产生沉淀
(5)芳香化合物E(C8H10O2)与B的水解产物互为同分异构体,1molE可与2 mol NaOH反应,其核磁共振氢谱中有3组峰且峰面积之比为3:1:1,则E有___________种可能的结构(不考虑立体异构)。
(6)以CH3OH和CH3ONa为原料(其他试剂任选),设计制备CH3COCH2 COOCH3的合成路线:CH3OH![]() ______。
______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物结构如图,下列说法中正确的是

A. 该物质的化学式为C15H12O8BrCl
B. 该物质能与FeCl3溶液发生显色反应
C. 1mol该物质最多能与3mol溴水发生加成反应
D. 一定条件下,1mol该物质最多能与7molNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com