

| A. | ①装置中阴极处产生的气体能够使湿润的淀粉KI试纸变蓝 | |
| B. | ②装置不能完成在铁制品上镀铜 | |
| C. | ③装置中电子由b极流向a极 | |
| D. | ④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
分析 A、①装置是电解池,阴极是阳离子得到电子发生还原反应;
B、②装置待镀制品和电源负极相连做电解池的阴极;
C、③装置是原电池,电子流向是从负极经导线流向正极;
D、④装置离子交换膜允许离子通过,氯气不能通过.
解答 解:A、①装置是电解池,阴极是溶液中阳离子得到电子发生还原反应,应是铜离子得到电子生成铜,故A错误;
B、②装置待镀制品和电源负极相连做电解池的阴极;故B错误;
C、③装置是原电池,电子流向是从负极经导线流向正极,即从a极流向b极,故C错误;
D、④装置中的离子交换膜允许离子通过,氯气不能通过,可以避免生成的Cl2与NaOH溶液反应,故D正确;
故选D.
点评 本题考查了电解池、原电池工作原理的应用,电极名称、电极判断、电极反应、电子流向、电解应用等基础知识,熟练掌握基础是解题关键.


科目:高中化学 来源: 题型:选择题
| A. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| B. | 可燃性气体点燃或加热之前应验纯,以防爆炸 | |
| C. | 浓NaOH溶液溅到皮肤上,立即用稀H2SO4冲洗 | |
| D. | 用蒸发的方法将自来水制成蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol•L-1 NaOH溶液 | B. | 2 mol•L-1HCl溶液 | ||
| C. | 2 mol•L-1NaCl溶液 | D. | 硅酸胶体(胶粒带负电荷) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2(b-2a)mol•L-1 | B. | 20(b-2a)mol•L-1 | C. | 20 (b-a) mol•L-1 | D. | 20(2a-b) mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
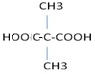 .
.查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上第二次适应性考试化学卷(解析版) 题型:选择题
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物: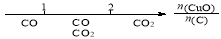
B.Fe在Cl2中的燃烧产物:
C.AlCl3溶液中滴加NaOH后铝的存在形式: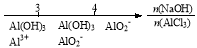
D. 氨水与SO2反应后溶液中的铵盐:
氨水与SO2反应后溶液中的铵盐: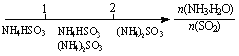
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

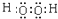 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com