
 CO3和KHCO3的混合物4.60 g,与1.00 mol/L的盐酸反应.
CO3和KHCO3的混合物4.60 g,与1.00 mol/L的盐酸反应. 2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表):
2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表):| 所需数据取值范围 | 生成CO2气体的体积 |
| 盐酸不足量时 | |
| 盐酸足量时 | |
 气体的体积大于________L,小于________L.
气体的体积大于________L,小于________L. 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
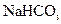 ,进而制取纯碱。主要装置如下:
,进而制取纯碱。主要装置如下: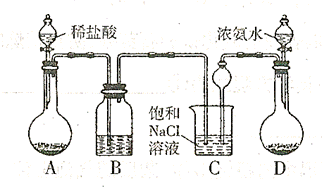
 ,则固体D可以是(只填一种 ;C装置中球形漏斗的作用是 。
,则固体D可以是(只填一种 ;C装置中球形漏斗的作用是 。 晶体可能含有的杂质有 ,用该
晶体可能含有的杂质有 ,用该 晶体制取纯碱时,有的杂质不会影响纯碱的纯度。原因是
晶体制取纯碱时,有的杂质不会影响纯碱的纯度。原因是  制取纯碱的化学方程式 。
制取纯碱的化学方程式 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
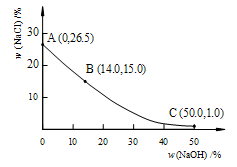
| A.20% | B.30% | C.45% | D. 55%。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
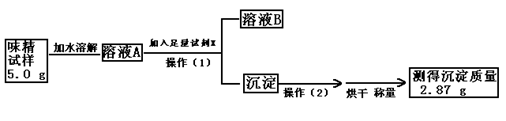 [
[ 是 。
是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.P1=P2 | B.P1=2P2 | C.P1=4P2 | D.P1=8P2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ol·L-1Na2CO3溶液,下列操作正确的是 ( )
ol·L-1Na2CO3溶液,下列操作正确的是 ( )| A.称取10.6 g无水碳酸钠,加入100 mL容量瓶中,加水溶解、定容 |
| B.称取10.6 g无水碳酸钠,加入100 mL蒸馏水,搅拌、溶解 |
| C.转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中 |
| D.定容后,塞好瓶塞,反复倒转、摇匀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com