
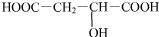 $→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O
$→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O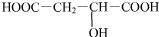 +2NaHCO3→
+2NaHCO3→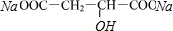 +2H2O+2CO2↑
+2H2O+2CO2↑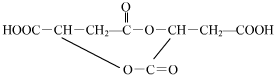 ,
, (或
(或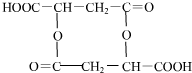 ).
). 分析 该酸中C、H、O的质量比为24:3:40,原子个数比为:$\frac{24}{12}$:$\frac{3}{1}$:$\frac{40}{16}$=4:6:5,其最简式为C4H6O5,该酸蒸气的密度是同温同压下氢气密度的67倍,相对分子质量为:67×2=134,由于最简式C4H6O5的式量为:12×4+6+16×5=134,则该酸分子式为:C4H6O5;0.lmol该酸与足量NaHCO3反应放出4.48L CO2,二氧化碳的物质的量为:$\frac{44.8L}{22.4L/mol}$=0.2mol,说明该酸分子中含有两个羧基;0.1mol该酸与足量金属Na反应放出3.36LH2,氢气的物质的量为:$\frac{33.6L}{22.4L/mol}$=0.15mol,说明该酸中含有2个羧基外,还应该含有1个羟基,又由于其分子中不含支链,则该酸的结构简式为: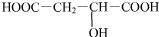 ,据此进行解答.
,据此进行解答.
解答 解:该酸中C、H、O的质量比为24:3:40,原子个数比为:$\frac{24}{12}$:$\frac{3}{1}$:$\frac{40}{16}$=4:6:5,其最简式为C4H6O5,该酸蒸气的密度是同温同压下氢气密度的67倍,相对分子质量为:67×2=134,由于最简式C4H6O5的式量为:12×4+6+16×5=134,则该酸分子式为:C4H6O5;0.lmol该酸与足量NaHCO3反应放出4.48L CO2,二氧化碳的物质的量为:$\frac{44.8L}{22.4L/mol}$=0.2mol,说明该酸分子中含有两个羧基;0.1mol该酸与足量金属Na反应放出3.36LH2,氢气的物质的量为:$\frac{33.6L}{22.4L/mol}$=0.15mol,说明该酸中含有2个羧基外,还应该含有1个羟基,又由于其分子中不含支链,则该酸的结构简式为: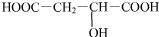 ,
,
(1)根据分析可知,该酸分子式为:C4H6O5,
故答案为:C4H6O5;
(2)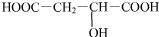 分子中含有羧基和羟基,在一定条件下分子内脱水生成不饱和脂肪酸:HOOCCH=CHCOOH,该反应化学方程式为:
分子中含有羧基和羟基,在一定条件下分子内脱水生成不饱和脂肪酸:HOOCCH=CHCOOH,该反应化学方程式为: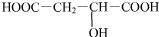 $→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O,
$→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O,
故答案为: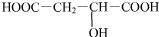 $→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O;
$→_{△}^{浓硫酸}$HOOCCH=CHCOOH+H2O;
(3)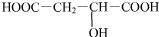 +2NaHCO3→
+2NaHCO3→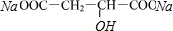 +2H2O+2CO2↑,
+2H2O+2CO2↑,
故答案为: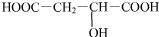 +2NaHCO3→
+2NaHCO3→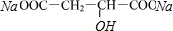 +2H2O+2CO2↑;
+2H2O+2CO2↑;
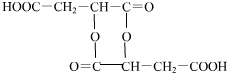
(4)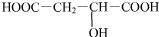 分子中含有两个羧基、1个羟基,在一定条件下每两个分子发生分子间脱水生成环酯,生成产物的结构简式有:
分子中含有两个羧基、1个羟基,在一定条件下每两个分子发生分子间脱水生成环酯,生成产物的结构简式有: 、
、 、
、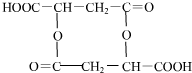 ,
,
故答案为: ;
; (或
(或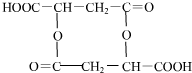 ).
).
点评 本题考查有机推断,题目难度中等,注意熟练掌握常见有机物结构与性质,根据题中信息确定该酸的分子式、结构简式为解答关键,试题侧重考查学生达到分析、理解能力及灵活应用基础知识的能力;(4)为难点,注意正确书写两分子该酸生成环酯的结构简式.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2溶液与CuSO4溶液反应:Ba2++SO42-=BaSO4↓ | |
| B. | NaOH溶液与稀硫酸的反应:OH-+H+=H2O | |
| C. | NaHCO3溶液与盐酸的反应:HCO3-+H+=H2O+CO2↑ | |
| D. | KCl溶液与AgNO3溶液的反应:Cl-+Ag+=AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )
A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系(部分反应物质已略去).A为一种金属单质,反应①②③均为化合反应,反应④为置换反应.下列有关说法不正确的是( )| A. | ①中所加试剂可能是氯气 | |
| B. | ③中需要加具有氧化性的试剂 | |
| C. | A与稀硝酸反应一定能实现元素M在①中发生的价态变化 | |
| D. | 元素M在②中发生的价态变化也能通过加碘化钾溶液实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用药匙取用粉末状或颗粒状固体 | B. | 用胶头滴管滴加少量液体 | ||
| C. | 倾倒液体时试剂瓶标签面向手心 | D. | 给盛有$\frac{2}{3}$体积液体的试管加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳的燃烧热等于110.5KJ/mol | |
| B. | 2C(s)+2O2(g)=2CO2(g);△H>-221 KJ/mol | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热为-57.3 KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出热量小于57.3 KJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com