
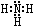 ��B����Ҳ��Z��X��Ԫ����ɣ���Ϊ���ͷɴ��Ļ��ȼ�ϣ���������һ��Һ̬�������֪�û��������Է�������Ϊ32������XԪ�ص���������Ϊ12.5%���Ҹ÷��ӽṹ��ֻ�е�������B�ĽṹʽΪ
��B����Ҳ��Z��X��Ԫ����ɣ���Ϊ���ͷɴ��Ļ��ȼ�ϣ���������һ��Һ̬�������֪�û��������Է�������Ϊ32������XԪ�ص���������Ϊ12.5%���Ҹ÷��ӽṹ��ֻ�е�������B�ĽṹʽΪ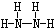 ����64g B������Һ̬˫��ˮǡ����ȫ��Ӧ�������������ֲ���Ⱦ��������̬���ʣ����ų�3000kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽN2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500kJ/mol��
����64g B������Һ̬˫��ˮǡ����ȫ��Ӧ�������������ֲ���Ⱦ��������̬���ʣ����ų�3000kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽN2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500kJ/mol������ ��1����ɵ����ʵĻ���Ԫ����C��H��O��N��Ԫ�أ���ԭ��������������֪X��Y��Z��L�ֱ�ΪH��C��N��O��
��2��N��H��Ԫ�ذ�ԭ����Ŀ��1��3�ɹ��ɷ���A��AΪNH3������������Nԭ�Ӻ�ÿ��Hԭ���γ�һ�����õ��Ӷԣ�Nԭ�ӻ�����һ���µ��Ӷԣ�
B����Ҳ��Z��X��Ԫ����ɣ���Ϊ���ͷɴ��Ļ��ȼ�ϣ���������һ��Һ̬������û��������Է�������Ϊ32������XԪ�ص���������Ϊ12.5%����BΪN2H4���Ҹ÷��ӽṹ��ֻ�е�������B��ÿ��Nԭ������2��Nԭ����Nԭ��֮�����һ�����ۼ����ݴ���дB�Ľṹʽ��
64gB�����ʵ�����2mol��2mol�º�˫��ˮ��ȫ��Ӧ���ɵ�����ˮ�ų�3000kJ����������1mol�º�˫��ˮ��Ӧ���ɵ�����ˮ�ų�1500kJȼ�ϣ��ݴ���д�÷�Ӧ���Ȼ�ѧ����ʽ��
��3��Se��������Ӧ��Ҫ���ϼ��Ȳ��ܷ�Ӧ�����Ը÷�Ӧ�����ȷ�Ӧ��Ԫ�صķǽ�����Խ���������յ�����Խ��
��� �⣺��1����������Ҫ����C��H��O��NԪ�أ�Lԭ�����������LΪOԪ�أ�XΪH��YΪC��ZΪNԪ�أ�
CԪ��ԭ�Ӻ�������У�δ�ɶԵ�������ɶԵ�����֮��Ϊ2��4=1��2��ԭ�ӵ��Ӳ���Խ�࣬��ԭ�Ӱ뾶Խ��ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ������������С������ԭ�Ӱ뾶��С˳����C��N��O��H��
�ʴ�Ϊ��O��1��2�� C��N��O��H��
��2��N��H��Ԫ�ذ�ԭ����Ŀ��1��3�ɹ��ɷ���A��AΪNH3������������Nԭ�Ӻ�ÿ��Hԭ���γ�һ�����õ��Ӷԣ�Nԭ�ӻ�����һ���µ��Ӷԣ������ʽΪ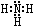 ��
��
B����Ҳ��Z��X��Ԫ����ɣ���Ϊ���ͷɴ��Ļ��ȼ�ϣ���������һ��Һ̬������û��������Է�������Ϊ32������XԪ�ص���������Ϊ12.5%����BΪN2H4���Ҹ÷��ӽṹ��ֻ�е�������B��ÿ��Nԭ������2��Nԭ����Nԭ��֮�����һ�����ۼ���B�ĽṹʽΪ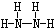 ��64gB�����ʵ�����2mol��2mol�º�˫��ˮ��ȫ��Ӧ���ɵ�����ˮ�ų�3000kJ����������1mol�º�˫��ˮ��Ӧ���ɵ�����ˮ�ų�1500kJȼ�ϣ��÷�Ӧ���Ȼ�ѧ����ʽΪN2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500 kJ/mol��
��64gB�����ʵ�����2mol��2mol�º�˫��ˮ��ȫ��Ӧ���ɵ�����ˮ�ų�3000kJ����������1mol�º�˫��ˮ��Ӧ���ɵ�����ˮ�ų�1500kJȼ�ϣ��÷�Ӧ���Ȼ�ѧ����ʽΪN2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500 kJ/mol��
�ʴ�Ϊ��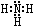 ��
��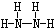 ��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500 kJ/mol��
��N2H4��l��+2H2O2��l��=N2��g��+4H2O��g����H=-1500 kJ/mol��
��3��Se��������Ӧ��Ҫ���ϼ��Ȳ��ܷ�Ӧ�����Ը÷�Ӧ�����ȷ�Ӧ��Ԫ�صķǽ�����Խ���������յ�����Խ�ǽ�����O��S��Se��Te������������������Ҫ����29.7kJ�������ʴ�Ϊ��b��
���� ���⿼���Ϊ�ۺϣ��漰�Ȼ�ѧ��Ӧ��ԭ�ӽṹ��Ԫ�������ɵ�֪ʶ�㣬��������ͬһ����Ԫ�����ʵݱ���ɡ�ԭ�ӽṹ��֪ʶ�㼴�ɽ����Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ������ѧ�ڵ����ε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��H2�ɽ���ҵ�����е�NO����ԭ��N2��������ת����ϵ��ͼ(ͼ�м�����λΪmol), ��NO(g)+H2(g)= N2(g)+H2O(g)�ġ�HΪ�� ��
N2(g)+H2O(g)�ġ�HΪ�� ��

A��0.5(a+b-c-d)kJ/mol B��0.5(c+a-d-b)kJ/mol
C��0.5(c+d-a-b)kJ/mol D. 0.5(c+d-a-b)kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
Ϊ��̽��AgNO3�������Ժ����ȶ���,ij��ѧ��ȤС�����������ʵ�顣
��.AgNO3��������
����������˿����AgNO3��Һ��,һ��ʱ�����˿ȡ����Ϊ������Һ��Fe����������,����Һ�е�Ag+������,����������ʵ�顣��ѡ�õ��Լ�:KSCN��Һ��K3[Fe(CN)6]��Һ����ˮ��
��1��������±�:
���� | ���� | ���� |
ȡ��������Ag+�����Һ���Թ���,����KSCN��Һ,�� | �� | ����Fe3+ |
ȡ��������Ag+�����Һ���Թ���,����� ,�� | �� | ����Fe2+ |
��ʵ����ۡ�Fe����������ΪFe2+��Fe3+
��.AgNO3�����ȶ���
����ͼ��ʾ��ʵ��װ��A����AgNO3����,��������ɫ����,��װ��D���ռ�����ɫ���塣����Ӧ������,�Թ��в�������Ϊ��ɫ��
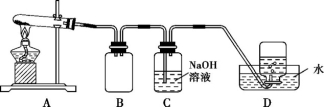

��2��װ��B�������� ��
��3����С�����۲���֤����ɫ����ΪO2,����֤������ ��
��4�����������ϡ�Ag2O�ͷ�ĩ״������Ϊ��ɫ;Ag2O�����ڰ�ˮ��
��������롿�Թ��в����ĺ�ɫ���������: ��.Ag; ��.Ag2O; ��.Ag��Ag2O��
��ʵ����֤����С��Ϊ��֤��������,�ֱ�ȡ������ɫ��������Թ���,����������ʵ�顣
ʵ���� | ���� | ���� |
a | ����������ˮ,�� | ��ɫ���岻�ܽ� |
b | ��������ϡ����,�� | ��ɫ�����ܽ�,����������� |
��ʵ�����ۡ���������ʵ��,����ȷ���������ɷֵ�ʵ���� (��ʵ����)��
��ʵ����ۡ���������ʵ����,д����С��ó�AgNO3�����ȷֽ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | ���� | ��ѧ�� | ���� | ��ѧ�� | ���� | ��ѧ�� | ���� |
| C-H | 414 | C-F | 489 | H-F | 565 | F-F | 158 |
| H-H | 436 | H-N | 391 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��� | ���� | ���� | ���� | |
| �¶�/�� | ���� | |||
| 1 | 40 | FeCl3��Һ | �� | �� |
| 2 | 20 | FeCl3��Һ | �� | �� |
| 3 | 20 | MnO2 | �� | �� |
| 4 | 20 | �� | �� | �� |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ������Ũ�ȵĹ�ϵ���㣺c��H+��=c��OH-��+c��CH3COO-�� | |
| B�� | 10mL0.01mol•L-1��CH3COOH��Һ�м�ˮϡ�ͣ���Һ��c��OH-����С | |
| C�� | �������Һ�м�������CH3COONa���壬ƽ�������ƶ� | |
| D�� | ������pH=2��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ���Һ��pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ࡢ��֬�������ʵ�ˮ����ﶼ�Ƿǵ���� | |
| B�� | ���ۺ���ά�صķ���ʽ��Ϊ��C6H10O5��n������Ϊͬ���칹�� | |
| C�� | ��ά�ء����ͷֱ���Ũ�������ʱ��Ũ����ķ�Ӧ����ͬһ���͵ķ�Ӧ | |
| D�� | �Ҵ�������ͱ��ӵķ����о����й�����-OH�����Ծ�����NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ��ѧʽ | ������ʼʱ��pH | ������ȫʱ��pH | �й����� |
| Co��OH��2 | 7.2 | 9.4 | Co+2HCl�TCoCl2+H2�� Co2++2NH3•H2O�TCo��OH��2��+2NH4+ Co2++2H2O?Co��OH��2+2H+ Ni+2HCl�TNiCl2+H2�� Ni2++6NH3•H2O�TNi��NH3��6]2++6H2O |
| Fe��OH��2 | 7.1 | 9.6 | |
| Fe��OH��3 | 2.3 | 3.7 | |
| Mg��OH��2 | 10.8 | 12.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com