
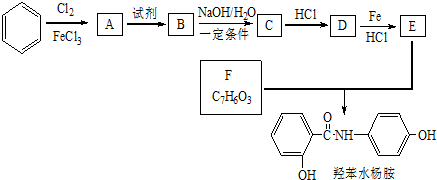
 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$
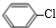 +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.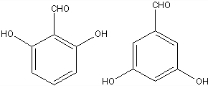 、
、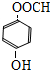 .
.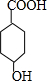 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$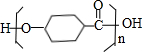 +(n-1)H2O.
+(n-1)H2O. 分析 由羟苯水杨胺结构简式、F的分子式可知,F为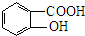 ,E为
,E为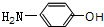 ,由反应信息逆推可知D为
,由反应信息逆推可知D为 ,由转化关系可知,苯与氯气发生取代反应生成A为
,由转化关系可知,苯与氯气发生取代反应生成A为 ,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为
,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为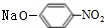 ,C酸化得到D,据此解答.
,C酸化得到D,据此解答.
解答 解:由羟苯水杨胺结构简式、F的分子式可知,F为 ,E为
,E为 ,由反应信息逆推可知D为
,由反应信息逆推可知D为 ,由转化关系可知,苯与氯气发生取代反应生成A为
,由转化关系可知,苯与氯气发生取代反应生成A为 ,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为
,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为 ,B发生水解反应生成C为
,B发生水解反应生成C为 ,C酸化得到D,
,C酸化得到D,
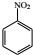
(1)D中硝基被还原生成氨基,则反应类型是还原反应,故答案为:还原;
(2)D为 ,其名称是对硝基苯酚,故答案为:对硝基苯酚;
,其名称是对硝基苯酚,故答案为:对硝基苯酚;
(3) ,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为
,A与浓硝酸、浓硫酸在加热条件下发生取代反应生成B为 ,反应方程式为
,反应方程式为 +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O,
+H2O,
故答案为: +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O;
+H2O;
(4)①F及同分异构体中组成元素相同,结构不同,由元素分析仪显示的信号(或数据)完全相同,
故选:C;
②F( )的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应,说明含有酚羟基、醛基,侧链为-OH、-OOCH时,有邻、间、对3种,侧链可为-CHO、2个-OH,2个-OH处于邻位,-CHO有2种位置,2个-OH处于间位,-CHO有3种位置,2个-OH处于对位,-CHO有1种位置,故符合条件的同分异构体共有9种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的结构简式为:
)的同分异构体中既能与FeCl3发生显色反应,又能发生银镜反应,说明含有酚羟基、醛基,侧链为-OH、-OOCH时,有邻、间、对3种,侧链可为-CHO、2个-OH,2个-OH处于邻位,-CHO有2种位置,2个-OH处于间位,-CHO有3种位置,2个-OH处于对位,-CHO有1种位置,故符合条件的同分异构体共有9种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:2:1的同分异构体的结构简式为: 、
、 ,
,
故答案为:9; 、
、 ;
;
③F为 ,F的同分异构体H的官能团与F相同,且苯环上的一溴取代产物只有两种,则羧基和酚羟基位于对位,H与足量氢气反应生成产物I,I为
,F的同分异构体H的官能团与F相同,且苯环上的一溴取代产物只有两种,则羧基和酚羟基位于对位,H与足量氢气反应生成产物I,I为 ,I发生缩聚反应方程式为n
,I发生缩聚反应方程式为n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +(n-1)H2O,
+(n-1)H2O,
故答案为:n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +(n-1)H2O.
+(n-1)H2O.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,涉及物质推断、方程式的书写、同分异构体种类判断等知识点,正确推断物质结构简式是解本题关键,注意限制型条件同分异构体种类判断,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:解答题
| 族 周 期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | h | i | |
| 4 | j | k |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 | |
| B. | 将一块未擦去氧化膜的铝片分别投入1 mol•L-1 CuSO4溶液中,铝片表面观察不到明显的反应现象 | |
| C. | 制取摩尔盐时和制取阿司匹林时都可用酒精洗涤产品 | |
| D. | 在AlCl3溶液中先滴加足量的NH4F溶液,在滴加氨水,将看不到溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述 | 评价 |
| A | 可用氢氧化钠醇溶液与硝酸酸化的硝酸银溶液鉴别烷烃与卤代烃 | 对.卤代烃都能与氢氧化钠醇溶液共热生成卤化钠.卤化钠与硝酸酸化的硝酸银溶液反应可生成卤化银沉淀 |
| B | 乙酸乙酯在H218O中水解,产物乙酸中将含有18O | 错,根据酯的水解规律,产物乙酸中将含有18O同位素.而乙醇則没有 |
| C | 不能用酸性高锰酸钾溶液除去甲烷中的乙烯气体 | 对.乙烯虽能与酸性高锰酸钾溶液反应,但会生成 CO2 |
| D | 可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和乙醛溶液 | 对.乙醇、乙酸和乙醛与新制的Cu(OH)2悬浊液反应现象皆不同.可以一次性鉴别 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )
某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )| A. | X原子可能为第VA族元素 | |
| B. | 该分子中既含有极性共价键又含有非极性共价键 | |
| C. | Y 原子可能为第ⅠA 族或第ⅦA 族元素元素 | |
| D. | 从圆球的大小分析,该分子可能为 N2F4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 150 mL 3 mol•L-1氯化钾溶液 | ||
| C. | 75 mL 2 mol•L-1氯化铵溶液 | D. | 50 mL 1 mol•L-1氯化铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
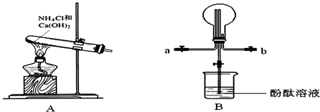
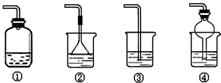
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com