
| A、原子半径:X>Y>Z |
| B、还原性:X->Y2->Z3- |
| C、非金属性:X>Y>Z |
| D、稳定性:ZH3>H2Y>HX |


科目:高中化学 来源: 题型:
| 选项 | 现象或事实 | 解释 |
| A | 用热的烧碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B | 漂白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所有反应都可以用四种基本反应类型进行概括 |
| B、氧化还原反应可能是复分解反应 |
| C、氧化还原反应可能是化合反应,也可能是分解反应 |
| D、置换反应可能不是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有① | B、只有①② |
| C、只有②③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最外层电子数相同 |
| B、都是双原子分子 |
| C、电子层数不同 |
| D、卤化氢中卤素都是-1价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H5 OH |
| B、CH3CHO |
| C、C2H4 |
| D、C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B、pH=3的盐酸和pH=11的氨水等体积混合,溶液显碱性 |
| C、0.1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一个H-H键断裂的同时有两个H-I键形成 |
| B、v (H2)正=v (HI)逆时的状态 |
| C、恒温恒容时,反应混合物总质量保持不变的状态 |
| D、恒温恒容时,体系的颜色不再发生变化的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
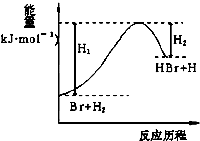 参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )| A、正反应为放热反应 |
| B、断键吸收的总能量大于成键放出的总能量 |
| C、反应物总能量高于生成物总能量 |
| D、升高温度可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com