
【题目】配合物Fe(CO)5的熔点一20℃,沸点103℃。可用于制备纯铁。Fe(CO)5的结构如图所示。
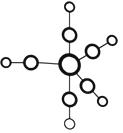
(1)基态Fe原子的价电子排布式是_____________________;Fe(CO)5晶体类型属于__________晶体。
(2)CO分子中C、O原子都满足8电子稳定结构,CO分子的结构式是________,写出与CO互为等电子体的分子的电子式:___________________。
(3)C、O、Fe的第一电离能由大到小的顺序为_______________________。
(4)关于Fe(CO)5,下列说法正确的是______。
A. Fe(CO)5是非极性分子,CO是极性分子 B. Fe(CO)5中Fe原子以sp3杂化方式与CO成键
C.1molFe(CO)5含有10mol配位键 D.Fe(CO)5==Fe+5CO反应中没有新化学键生成
(5)铁的三种晶体的晶胞均为立方晶胞,三种晶体的晶胞如下图所示。
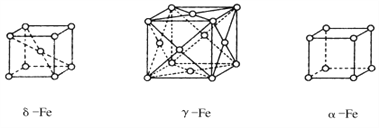
①上述三种晶体的晶胞中属于面心晶胞的是______(填“a”“δ””或“γ”)-Fe。
②a-Fe晶胞中铁原子的配位数为_______________。
③γ-Fe晶胞的边长为apm,则γ-Fe单质的密度为____g/cm3(NA表示阿伏伽德罗常数的值,列出计算式即可)。
【答案】 3d64s2 分子 C![]() O
O ![]() O>C>Fe A、C γ 6 ρ=(224/a3·NA)×1030(或ρ=[4×56/a3·NA]×1030)
O>C>Fe A、C γ 6 ρ=(224/a3·NA)×1030(或ρ=[4×56/a3·NA]×1030)
【解析】(1)铁为26号元素,基态Fe原子的价电子排布式为3d64s2;Fe(CO)5的溶点-20℃,沸点103℃,熔沸点较低,Fe(CO)5晶体属于分子晶体,故答案为:3d64s2;分子;
(2) CO分子中C、O原子都满足8电子稳定结构,CO分子的结构式为C≡O,与CO互为等电子体的分子有N2,故答案为:C≡O;N2;
(3)C、O、Fe三种元素的原子中铁的原子半径最大,Fe原子的价电子排布式为3d64s2,失去1个电子生成3d54s2,结构更稳定,第一电离能最小,C、O是同一周期元素,同一周期,从左到右,第一电离能逐渐增大,第一电离能由大到小的顺序为O>C> Fe,故答案为:O>C> Fe;
(4)A.根据Fe (CO)5的结构可知, Fe(CO)5为三角双锥结构,分子中正负电荷分布均匀,是非极性分子,CO中正负电荷分布不均匀,是极性分子,故A正确;B.Fe(CO)5中Fe原子与5个CO成键,不是sp3杂化,故B错误;C. 1molFe(CO)5 中Fe原子与5个CO形成5个配位键,在每个CO分子中存在1个配位键,共含有10mol配位键,故C正确;D. Fe(CO)5=Fe+5CO属于化学变化,包括化学键的断裂与形成,断开了分子中的配位键,形成了金属键,故D错误;故选AC;
(5)①根据晶胞结构图,三种晶体的晶胞中属于面心晶胞的是γ,故答案为:γ;
②α晶胞中晶胞顶点的铁原子与周围的6个铁原子距离相等且最小,配位数为6,故答案为:6;
③γ晶体晶胞的边长为a pm,1个晶胞中含有的铁原子数目=8×![]() +6×
+6×![]() =4,则γ-Fe单质的密度=
=4,则γ-Fe单质的密度=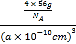 =
=![]() g/cm3,故答案为:
g/cm3,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】甲、乙两同学用一种标准盐酸去测定同一种未知浓度的NaOH溶液的浓度,但操作不同;甲把一定体积的NaOH溶液放入锥形瓶,把标准盐酸放入滴定管进行滴定;乙把一定体积的标准盐酸放入锥形瓶,把未知液NaOH溶液放入滴定管进行滴定。
(1)甲同学使用的是_______滴定管,乙同学使用的是________滴定管。
(2)甲同学的滴定管在用蒸馏水洗净后没有用标准盐酸润洗,乙同学的滴定管在用蒸馏水洗净后也没有用待测NaOH溶液润洗,其余操作均正确,这样甲同学测定结果________(偏大、偏小、无影响,下同),乙同学测定结果__________。
(3)乙同学选择酚酞作指示剂进行试验,如何来判断滴定终点:____________。
(4)甲同学根据三次实验分别记录有关数据如下:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据计算c(NaOH)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯,反应装置如图。下列对该实验的叙述错误的是

A.长玻璃管起冷凝回流作用
B.水浴加热其优点是受热均匀,便于控制温度
C.粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤
D.洗涤后,用无水CaCl2干燥,然后过滤,得到纯硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组采用碘量法测定河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2![]() +I2 = 2I+
+I2 = 2I+![]() )。
)。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____。
(2)“氧的固定”中发生反应的化学方程式为___________。
(3)Na2S2O3能水解,则滴定时Na2S2O3溶液应装在_____(填下图中的仪器编号)。请补充润洗该仪器的操作方法:从滴定管____加入3~5mL所要盛装的溶液,__________,然后,一手控制活塞(酸式滴定管轻轻转动活塞;碱式滴定管轻轻挤压玻璃球),将液体从滴定管__放入预置的烧杯中。
甲 乙
乙 丙
丙![]() 丁
丁![]()
(4)某次滴定前滴定管液面如图所示,读数为________mL。
![]()
(5)量取100.00 mL水样经固氧、酸化后,从中取20.00 mL放入锥形瓶,用a mol·L1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为________________;若消耗Na2S2O3溶液的体积为b mL,则水样中溶解氧的含量为__mg·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
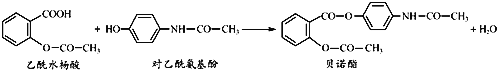
下列有关叙述正确的是
A.贝诺酯分子中有三种含氧官能团
B.贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
C.乙酰水杨酸和对乙酰氨基酚均能与Na2CO3溶液反应放出CO2气体
D.可用FeCl3 溶液区别乙酰水杨酸和对乙酰氨基酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2H2(g)+O2(g) ![]() 2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g)
2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq)
2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq) ![]() H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
H2O(l) H= -57.3 kJ·mol-1。据此判断下列说法正确的是
A. CH3OH的燃烧热为1452 kJ·mol-1
B. 2H2(g)+O2(g) ![]() 2H2O(g) H > -571.6 kJ·mol-1
2H2O(g) H > -571.6 kJ·mol-1
C. CH3COOH(aq)+NaOH(aq) ![]() H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
D. 2CH3OH(l)+O2(g) ![]() 2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中正确的是( )
A.配制一定物质的量浓度的![]() 溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释
溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释
B.![]() 溶液的物质的量浓度为
溶液的物质的量浓度为![]() ,用水稀释到物质的量浓度为
,用水稀释到物质的量浓度为![]() ,需要水
,需要水![]()
C.配制一定物质的量浓度的氯化钾溶液:准确称取一定质量的氯化钾固体,放入![]() 的容量瓶中,加入
的容量瓶中,加入![]() 溶解,振荡摇匀
溶解,振荡摇匀
D.将![]() 溶解在
溶解在![]() 水中,配制溶质质量分数为10%的
水中,配制溶质质量分数为10%的![]() 溶液
溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根皮素J(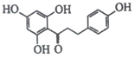 )是国外新近研究开发出来的一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下:
)是国外新近研究开发出来的一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下:
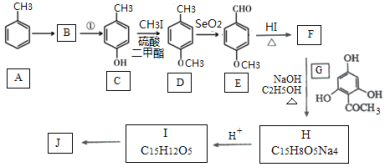
已知:
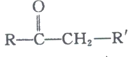 +R’’CHO
+R’’CHO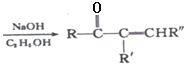 +H2O
+H2O
回答下列问题:
(1)C的化学名称是___________.E中的官能团的名称为_______________.
(2)B为溴代烃,请写出A→B的反应条件___________.
(3)写出由C生成D和由D生成E的反应类型___________、___________.
(4)F→H的化学方程式为______________________.
(5)M是E的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构)
①能与FeCl3溶液发生显色反应 ②能发生银镜反应
(6)设计以丙烯和1,3-丙二醛为起始原料制备![]() 的合成路线_______(无机试剂任选).
的合成路线_______(无机试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol/(L·min)]表示,则正确的关系式是
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol/(L·min)]表示,则正确的关系式是
A. 4v(NH3)=5v(O2) B. 5v(O2)=6v(H2O) C. 2v(NH3)=3v(H2O) D. 4v(O2)=5v(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com