
【题目】一定温度下,冰醋酸加水稀释过程中溶液的导电能力实验结果如图所示:
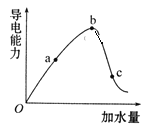
(1)“O”点为什么不导电?____________。
(2)比较a、b、c三点的c(H+)大小。____________(用“﹥”“=” 或“﹤”)
(3)a、b、c三点中,醋酸的电离程度最大的是哪一点?____________。
(4)若要使c点溶液中的c(CH3COO-)增大,试列举两条可行的措施______。
(5)在稀释过程中,c(H+)、n(H+)、c(OH-)和n(CH3COOH)中,始终保持增大趋势的是_________。
【答案】冰醋酸还没有电离 b>a>c c 加热 ,加CH3COONa固体(或其它合理答案 n(H+),c(OH-)
【解析】
从图中可以看出,从0点到b点,溶液的导电能力增强,说明溶液中离子浓度增大;从b点到c点,溶液的导电能力减弱,说明溶液中离子浓度减小。
(1)在“O”点,只有冰醋酸,冰醋酸不发生电离,不存在自由离子,所以不导电。
答案为:冰醋酸还没有电离
(2从导电能力看,导电能力b>a>c,则溶液中c(H+)关系为b>a>c。答案为:b>a>c
(3)从a点到b点,再到c点,醋酸中不断加水,醋酸不断稀释,浓度不断减小,所以电离程度不断增大,电离程度最大的是c点。答案为:c
(4)若要使c点溶液中的c(CH3COO-)增大,可采取的措施是加热、加CH3COONa固体,也可加入冰醋酸。
答案为:加热、加CH3COONa固体等。
(5)在稀释过程中,n(H+)、c(OH-)增大,c(H+)、n(CH3COOH)减小,始终保持增大趋势的是n(H+)、c(OH-)。答案为:n(H+)、c(OH-)


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.苯与溴水、酸性高锰酸钾溶液不反应,说明苯分子中碳原子间只存在单键
B.煤是由有机物和无机物所组成的复杂的混合物
C.相同质量的烷烃完全燃烧时,甲烷的耗氧量最高
D.乙烯可在催化剂作用下与H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体![]() 血液的pH需控制在7.35~7.45之间,过高过低都会引起身体不适,甚至危及生命。人体血液能维持在稳定的pH范围主要是人血浆中一定浓度的
血液的pH需控制在7.35~7.45之间,过高过低都会引起身体不适,甚至危及生命。人体血液能维持在稳定的pH范围主要是人血浆中一定浓度的![]() 和
和![]() 起调节作用。按要求回答下列问题。
起调节作用。按要求回答下列问题。
(1)用离子方程式解释血液呈弱碱性的原因____;
(2)当血液的![]() (即
(即![]() 浓度为
浓度为![]() )时,
)时,![]() 和
和![]() 浓度比值约为20:1,计算出此时碳酸的
浓度比值约为20:1,计算出此时碳酸的![]() 7.96×10-7,查阅资料得常温下碳酸的
7.96×10-7,查阅资料得常温下碳酸的![]() ,解释与计算所得数据存在差异的原因____。
,解释与计算所得数据存在差异的原因____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z原子序数依次增大,X元素基态原子有2个未成对电子,Y元素基态原子的核外p电子数比s电子数少1个,Z的一种超原子![]() 具有40个价电子,下列说法错误的是( )
具有40个价电子,下列说法错误的是( )
A.![]() 的空间构型为平面三角形
的空间构型为平面三角形
B.简单离子半径:![]()
C.![]() 中心原子的杂化方式为
中心原子的杂化方式为![]() 杂化
杂化
D.化合物ZY的结构与X的某种单质的结构相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe(s)+CO2(g) ![]() FeO(s)+CO(g) △H=akJ/mol,平衡常数为K;测得在不同温度下,K值如下:
FeO(s)+CO(g) △H=akJ/mol,平衡常数为K;测得在不同温度下,K值如下:
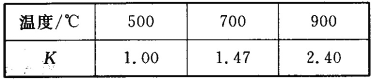
(1)若500℃时进行上述反应,CO2起始浓度为1 mol/L,CO的平衡浓度为_____。
(2)方程式中的a________0(填“大于”“小于”或“等于”)。
(3)900℃上述反应达到平衡,要使得该平衡向左移动,其他条件不变时,可以采取的措施有________(填序号)
A.缩小反应器体积 B.加入FeO
C.降低温度到500℃ D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种红色固体,常用作示温涂料。制备反应为:
是一种红色固体,常用作示温涂料。制备反应为:![]()
![]() 。下列说法正确的是( )
。下列说法正确的是( )
A.上述反应的产物![]() 中,Hg的化合价为
中,Hg的化合价为![]()
B.上述反应中Hg元素与Cu元素均被还原
C.上述反应中生成![]() 时,转移的电子数为
时,转移的电子数为![]()
D.由以上信息可推知:可发生反应![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能作为一种清洁高效的二次能源,在未来能源格局中发挥着重要作用。已知:常温下,![]()
![]()
![]() ,
,![]() 。回答下列问题:
。回答下列问题:
(1)常温下、水的分解不能自发进行的热力学依据是________________________。
(2)将![]() 负载在
负载在![]() 上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应
上,产氧温度在1200℃,产氢温度在1000℃时,可顺利实现水的分解,氢气产量高且没有明显的烧结现象。循环机理如下,过程如图1所示,不考虑温度变化对反应![]() 的影响。
的影响。
第Ⅰ步:![]()
![]()
![]()
第Ⅱ步:![]()
![]()
![]()

①![]() _________285.84(填“>”“<”或“=”)。第Ⅰ步反应中化合价有变化的元素为________(填名称)。
_________285.84(填“>”“<”或“=”)。第Ⅰ步反应中化合价有变化的元素为________(填名称)。
②第Ⅱ步反应的![]() ,
,![]() ,
,![]() 、
、![]() 分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入2mol
分别为正、逆反应速率常数,仅与温度有关。1000℃时,在体积为1L的B反应器中加入2mol![]() 发生上述反应,测得
发生上述反应,测得![]() 和
和![]() 物质的量浓度随时间的变化如图2所示,则60min内,
物质的量浓度随时间的变化如图2所示,则60min内,![]() _________
_________![]() (保留2位小数)。a点时
(保留2位小数)。a点时![]() ________(填最简整数比);平衡时,体系压强为10kPa,则
________(填最简整数比);平衡时,体系压强为10kPa,则![]() _________。
_________。
(3)热力学铜-氯循环制氢法分电解、水解、热解三步进行。

电解:![]() ;
;
水解:![]() ;
;
热解:![]() 。
。
已知:![]() 为白色固体,
为白色固体,![]() 。
。
电解装置如图所示,则A为________极(填“阳”或“阴”),B极电极反应为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A可进行如下转化:

回答下列问题:
(1)B的化学名称为_____.
(2)由C合成涤纶的化学方程式为_____.
(3)E的苯环上一氯代物仅有两种,E的结构简式为_____.
(4)写出A所有可能的结构简式_____.
(5)写出符合下列条件的E的同分异构体的结构简式_____.
①核磁共振氢谱显示苯环上仅有两种氢 ②可发生银镜反应和水解反应.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com