
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
 2CO2+N2
2CO2+N2| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1Com] |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |

| 试剂组合序号 | 固体试剂(g) | NH3体积(ml) | |
| a | 12.0gCa(OH)2(过量) | 10.8gNH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0gNaOH(过量) | 10.8gNH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0gCaO(过量) | 10.8gNH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
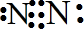
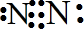
| ||
| ||
 ②氨气可使湿润的红色的石蕊试纸变蓝的原因(用方程式表示)
②氨气可使湿润的红色的石蕊试纸变蓝的原因(用方程式表示)
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1 |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) | |
| a | 12.0g Ca(OH)2(过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0g NaOH(过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0g CaO(过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |
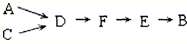
查看答案和解析>>
科目:高中化学 来源:大纲版2012届高三上学期单元测试(3)化学试题 题型:058
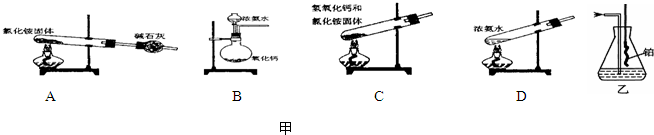
回答实验室制取NH3并进行氨气性质实验的若干问题,根据要求填写空白.
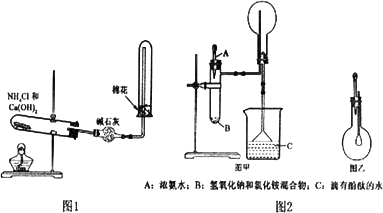
(1)实验室用图1所示装置制备干燥的NH3:
①反应的化学方程式为:________.装置中收集NH3的试管口放置棉花团的作用是:________.
②干燥管中干燥剂能否改用无水CaCl2________,理由是________.
(2)图2是某化学小组制备NH3并进行性质实验时的改进装置.按图甲把仪器安装好,称取2 g固体氯化铵装入试管底部,再快速称取2 g氢氧化钠覆盖在氯化氨上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2 mL浓氨水);烧杯内盛满有酚酞试液的水;把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.
将图甲中收满NH3的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先吸入2 mL H2O,此时小气球系在玻璃棒上呈自然松弛状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某项性质.
①下面是某同学关于某化学小组能用图甲制取NH3的原因分析,有道理的是________.
a.在NH3·H2O中有平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-,NaOH使平衡向左移动
+OH-,NaOH使平衡向左移动
b.在NH3·H2O中有平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-,NH4Cl使平衡向左移动
+OH-,NH4Cl使平衡向左移动
c.NaOH溶于水时放热,使体系的温度升高,NH3的溶解度减小,会有部分NH3逸出
d.NH4Cl与NaOH在此情况下可反应生成NH3,即NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
e.NH4Cl会分解释放出NH3
②图甲中的NH4Cl与NaOH固体混合物能否用CaO固体代替?________(填“能”或“不能”).
③如何判断图甲中烧瓶已收满NH3?________.
④图乙中随胶头滴管中的水挤入烧瓶中,观察到的现象是________,说明NH3________.
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(15分)(1)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
2NO+2CO 2CO2+N2
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 | T/℃ | NO初始浓度 mol·L-1 | CO初始浓度 mol·L-1 | 催化剂的比表面积 ㎡·g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ |
|
|
| 124 |
| Ⅲ | 350 |
|
| 124 |
①请在表格中填入剩余的实验条件数据。
②设计实验Ⅱ、Ⅲ的目的是 。
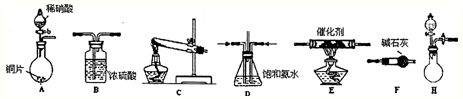
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质。某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程。提供的装置:
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是: (填装置序号)。
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
分析表中数据,实验室制NH3产率最高的是 (填序号),其它组合NH3产率不高的原因是 。
步骤二、模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式: 。
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是: 。
③D装置中的液体可换成 (填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com