
| A. | 1:2:3 | B. | 3:2:1 | C. | 1:1:1 | D. | 6:3:2 |
分析 体积相同、物质的量浓度相同的(NH4)3PO4、(NH4)2HPO4和NH4H2PO4溶液中各溶质的物质的量相等,与NaOH溶液分别发生反应:(NH4)3PO4+3NaOH=Na3PO4+3NH3•H2O、(NH4)2HPO4+3NaOH=Na3PO4+H2O+2NH3•H2O、NH4H2PO4+3NaOH=Na3PO4+2H2O+NH3•H2O,由方程式可知消耗的NaOH的物质的量相等,再根据v=$\frac{n}{c}$进行判断.
解答 解:体积相同、物质的量浓度相同的(NH4)3PO4、(NH4)2HPO4和NH4H2PO4溶液中各溶质的物质的量相等,与NaOH溶液分别发生反应:(NH4)3PO4+3NaOH=Na3PO4+3NH3•H2O、(NH4)2HPO4+3NaOH=Na3PO4+H2O+2NH3•H2O、NH4H2PO4+3NaOH=Na3PO4+2H2O+NH3•H2O,由方程式可知消耗的NaOH的物质的量相等,NaOH的浓度相同,故消耗NaOH溶液的体积相等,即三者与物质的量浓度相等的氢氧化钠溶液完全反应所需要的体积比为1:1:1,
故选C.
点评 本题考查物质的量浓度有关计算,难度不大,清楚发生的反应式解题的关键,注意利用方程式进行计算.


科目:高中化学 来源: 题型:选择题
| A. | 7.8 g Na2O2中含有的阴离子数为0.1NA | |
| B. | 常温下,含0.1 mol碳酸钠的溶液中含有CO${\;}_{3}^{2-}$的个数为0.1NA | |
| C. | 7.8 g Na2S和Na2O2的混合物中,含有的阳离子数目为0.1NA | |
| D. | 12 g NaHSO4晶体中阳离子和阴离子的总数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、SO42-、Cl-、Na+ | B. | OH-、K+、NO3-、Ba2+ | ||
| C. | Na+、CO32-、Ca2+、Cl- | D. | Mg2+、SO42-、Al3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Fe(NO3)3 溶液中滴入少量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| B. | 向AlCl3 溶液中加入足量氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Cu(OH)2沉淀溶于氨水得到深蓝色溶液:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O | |
| D. | 澄清石灰水中加入少量NaHCO3 溶液:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅烷的分子通式可表示为SinH2n+2 | B. | 甲硅烷燃烧生成SiO2和H2O | ||
| C. | 甲硅烷的沸点高于甲烷 | D. | 甲硅烷的稳定性比甲烷强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
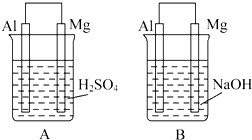 有A、B两位学生均想利用原电池反应验证金属的活动性顺序,并探究产物的有关性质.分别设计如图所示的原电池,请完成以下问题:
有A、B两位学生均想利用原电池反应验证金属的活动性顺序,并探究产物的有关性质.分别设计如图所示的原电池,请完成以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com