

分析 (1)根据仪器的特点确定仪器的名称;
(2)二氧化硫具有还原性,能使高锰酸钾褪色,还具有氧化性,能和氢硫酸之间反应得到单质硫;
(3)二氧化硫的密度大于空气,就可选择向上排空气法收集,具有毒性,要进行尾气处理.
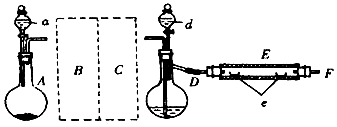
解答 解:(1)根据仪器的特点知道仪器A的名称是分液漏斗,故答案为:分液漏斗;
(2)高锰酸钾具有强氧化性,二氧化硫具有还原性,能使高锰酸钾溶液褪色,能和氢硫酸之间反应得到单质硫,反应为2H2S+SO2=3S↓+2H2O,体现二氧化硫的氧化性,
故答案为:溶液褪色;b;2H2S+SO2=3S↓+2H2O;a;
(3)二氧化硫的密度大于空气,就可选择向上排空气法,收集收集SO2气体可以选择的装置为ac,二氧化硫具有毒性,要进行尾气处理,可以用氢氧化钠来吸收,
故答案为:ac;NaOH.
点评 本题是一道考查学生二氧化硫性质的实验方案设计题,考查学生分析和解决问题的能力,难度不大.


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:实验题

| 操 作 | 现 象 |
| 取0.1mol/L的FeBr2溶液100mL,测溶液的pH | pH试纸变红(约为4) |
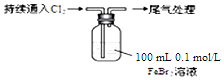 | ⅰ.开始通入100mLCl2(折合标准状况),溶液由浅绿色逐渐变黄; ⅱ.稍后,继续通入Cl2,溶液黄色加深,变为棕黄色; iii.稍后,溶液由棕黄色变浅,最终变为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成酚醛树脂的单体是苯酚和甲醇 | |
| B. | 汽油和乙烯均为石油分馏得到的产品 | |
| C. | 塑料、合成纤维和合成橡胶都属于合成材料 | |
| D. | 蔗糖、淀粉、油脂水解均能生成电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
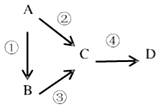 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如下转化关系,其中A是单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 846.3 kJ•mol-l | B. | 758.3 kJ•mol-l | C. | 890.3 kJ•mol-l | D. | 714.3 kJ•mol-l |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使甲基橙呈红色的溶液中:K+、Ba2+、OH-、AlO2- | |
| B. | 由水电离出C(H+)=1×10-14溶液中:Ca2+、K+、Cl-、HCO3- | |
| C. | $\frac{C({H}^{+})}{C(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | C(Fe3+)=0.1mol/L的溶液中:K+、CO32-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中溶解性:Na2CO3<NaHCO3 | |
| B. | 与酸反应的剧烈程度:Na2CO3<NaHCO3 | |
| C. | 热稳定性:Na2CO3>NaHCO3 | |
| D. | 二者间在一定条件下可相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Na+、NO3-、CO32- | B. | Mg2+、Cl-、Na+、SO42- | ||
| C. | K+、Cl-、HCO3-、NO3- | D. | Ca2+、Na+、Fe3+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com