
| A.25 ℃时,醋酸钠溶液呈碱性 |
| B.25 ℃时,0.1 mol·L-1的醋酸的pH约为3 |
| C.25 ℃时,等体积的盐酸和醋酸,前者比后者的导电能力强 |
| D.25 ℃时,将pH=3的盐酸和醋酸稀释成pH=4的溶液,醋酸所需加入的水多 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.K+、HCO3-、CO32-、Br- | B.SO32-、HSO3-、OH-、K+ |
| C.Fe3+、Cu2+、NO3-、SO32- | D.H+、Na+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
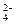 、SO
、SO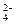 四种离子中的一种或几种。取少量这种溶液分别盛于三支试管中,进行如下实验:
四种离子中的一种或几种。取少量这种溶液分别盛于三支试管中,进行如下实验:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用干燥洁净的铂丝蘸取溶液,在火焰上灼烧,若火焰呈黄色,证明不含K+ |
| B.向溶液中加入新制氯水和CCl4,振荡、静置,若上层溶液呈紫红色,证明含有I— |
| C.向溶液中先加入新制氯水,再加入KSCN溶液,若溶液呈血红色,证明含有Fe2+ |
| D.向溶液中加入氢氧化钠溶液,若立即产生红褐色沉淀,证明含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑤ | B.①②③ | C.②④ | D.①③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
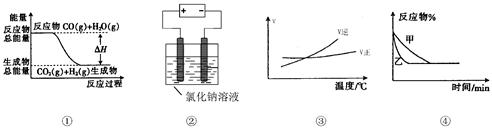
A.图①表示可逆反应“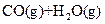  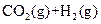 ”中的 ”中的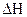 小于0 小于0 |
| B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极能收集到的气体体积之比一定为1:1 |
C.图③表示可逆反应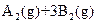  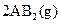 的 的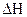 大于0 大于0 |
D.图④表示压强对可逆反应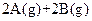  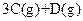 的影响,乙的压强大 的影响,乙的压强大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合: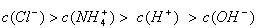 |
B.10mL1mol/LNH4Cl溶液与5mL2mol/LNaOH溶液混合: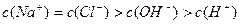 |
C.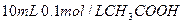 溶液与 溶液与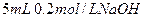 溶液混合: 溶液混合: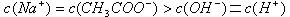 |
| D.将pH=3的盐酸与pH=11的氨水等体积混合后: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含有0.1mol/Lca2+的溶液中:Na+、K+、ClO-、Cl- |
B.在pH=12的溶液中:NH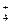 、Na+、SO 、Na+、SO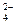 、Cl- 、Cl- |
C.在c(H+)=0.1mol/L的溶液中:K+、I-、Cl-、NO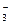 |
D.在澄清透明的无色溶液中:Na+、Cu2+、Cr2O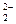 、NO 、NO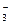 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.在稀氨水中加水稀释, 会增大 会增大 |
| B.若酸性HA>HB,则等物质的量浓度等体积的NaA和NaB溶液混合有关系: c(OH-)>c(A-)>c(B-)>c(H+) |
| C.0.1 mol·L-1的一组溶液pH由大到小排列为: NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| D.分别稀释10mLpH=1的盐酸和醋酸至100mL,后者pH变化大,说明醋酸是弱酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com