
 二氧化硫(SO2)是中学化学中常见的气体,在生产生活中用途广泛,某化学课题小组对其进行了实验探究,方案如下:
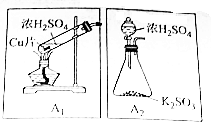
二氧化硫(SO2)是中学化学中常见的气体,在生产生活中用途广泛,某化学课题小组对其进行了实验探究,方案如下:分析 SO2中S元素的化合价为+4价,为中间价态,既有氧化性也具有还原性,由实验装置可知,A1图中发生Cu与浓硫酸的反应制备二氧化硫,A2装置中发生浓硫酸与亚硫酸钾的反应制备二氧化硫,A1图中需要加热,浓硫酸变为稀硫酸时与Cu不反应,A2装置中分液漏斗可控制液体的滴加速度,以此来解答.
解答 解:(1)硫元素的化合价最低为-2价,最高为+6价,SO2中S元素的化合价为+4价,为中间价态,预测SO2的化学性质有氧化性和还原性,
故答案为:氧化性;还原性;
(2)①A1图中为Cu与浓硫酸反应,其化学反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
②与A1装置相比,A2装置的优点是不用加热,相对安全,易于控制反应进行,反应更充分,故答案为:不用加热,相对安全,易于控制反应进行,反应更充分.
点评 本题考查二氧化硫的制备实验及评价,为高频考点,把握制备原理及实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
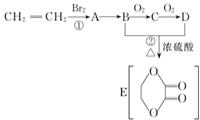 由乙烯和其他无机原料合成环状酯,其合成过程如下(水及其他无机产物均已省略)
由乙烯和其他无机原料合成环状酯,其合成过程如下(水及其他无机产物均已省略)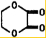 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
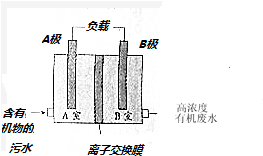
| A. | A极上发生类似C6H10O5-24e+7H2O═6CO2↑+24H+的电极反应 | |
| B. | B极上发生的是还原反应,工作过程中电极周围溶液的pH增大 | |
| C. | 工作过程中外电路的电子由A极流向B极,溶液中则由B极流向A极 | |
| D. | 污水中所存在的阳离子经离子交换膜由A室流向B室. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu、CuSO4、正极 | B. | Cu、CuCl2、负极 | C. | CuCl2、Cu、正极 | D. | Cu、CuSO4、负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.
向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com