
| A. | 反应过程中得到8.96 L的气体 | B. | 最终得到的溶液中溶质为NaCl | ||
| C. | 最终Al元素全部以沉淀形式存在 | D. | 最终得到的溶液中n(NaCl)=0.3 mol |
分析 15.6gNa2O2的物质的量为$\frac{15.6g}{78g/mol}$=0.2mol,5.4gAl的物质的量为:$\frac{5.4g}{27g/mol}$=0.2mol,首先发生反应2Na2O2+2H2O═4NaOH+O2↑,生成NaOH为0.4mol,再发生2Al+2NaOH+2H2O═2NaAlO2+3H2↑,由方程式可知Al完全反应,剩余NaOH为0.4mol-0.2mol=0.2mol,生成NaAlO2为0.2mol,通入标准状况下的HCl气体6.72L,物质的量为:$\frac{6.72L}{22.4L/mol}$=0.3mol,首先发生反应NaOH+HCl═NaCl+H2O,剩余HCl为0.3mol-0.2mol=0.1mol,再发生反应NaAlO2+HCl+H2O═Al(OH)3↓+NaCl,由方程式可知,NaAlO2有剩余,HCl完全反应,生成Al(OH)3为0.1mol,最终溶液中溶质为NaAlO2、NaCl,据此进行解答.
解答 解:15.6gNa2O2的物质的量为$\frac{15.6g}{78g/mol}$=0.2mol,5.4gAl的物质的量为:$\frac{5.4g}{27g/mol}$=0.2mol,首先发生反应2Na2O2+2H2O═4NaOH+O2↑,生成NaOH为0.4mol,再发生2Al+2NaOH+2H2O═2NaAlO2+3H2↑,由方程式可知Al完全反应,剩余NaOH为0.4mol-0.2mol=0.2mol,生成NaAlO2为0.2mol,通入标准状况下的HCl气体6.72L,物质的量为:$\frac{6.72L}{22.4L/mol}$=0.3mol,首先发生反应NaOH+HCl═NaCl+H2O,剩余HCl为0.3mol-0.2mol=0.1mol,再发生反应NaAlO2+HCl+H2O═Al(OH)3↓+NaCl,由方程式可知,NaAlO2有剩余,HCl完全反应,生成Al(OH)3为0.1mol,最终溶液中溶质为NaAlO2、NaCl,
A.过氧化钠与水反应生成氧气为0.2mol×$\frac{1}{2}$=0.1mol,铝与氢氧化钠反应生成氢气为0.2mol×$\frac{3}{2}$=0.3mol,故生成氢气的物质的量为:0.1mol+0.3mol=0.4mol,×没有指出在标准状况下,不能使用标准状况下的气体摩尔体积计算混合气体的体积,故A错误;
B.根据分析可知,最终得到溶质为NaAlO2、NaCl,故B错误;
C.由上述分析可知,Al元素以Al(OH)3、NaAlO2形式存在,故C错误;
D.通入HCl的物质的量为0.3mol,根据氯元素守恒可知最终得到氯化钠的物质的量为0.3mol,故D正确;
故选D.
点评 本题考查混合物反应的计算、钠的化合物与铝单质及化合物的性质等知识,题目难度中等,根据过量计算判断发生的反应是解题的关键,试题培养了学生的化学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

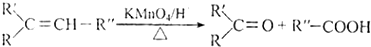
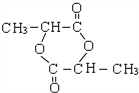
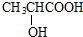 +HBr$\stackrel{△}{→}$CH3CHBrCOOH+H2O
+HBr$\stackrel{△}{→}$CH3CHBrCOOH+H2O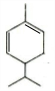 ,A与等物质的量的Br2进行加成反应的产物共有3种.(不考虑立体异构)
,A与等物质的量的Br2进行加成反应的产物共有3种.(不考虑立体异构)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: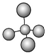 | B. | NH4Br的电子式: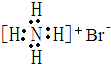 | ||
| C. | 34S2-的结构示意图: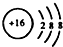 | D. | 邻羟基甲苯酸的结构简式: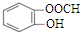 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
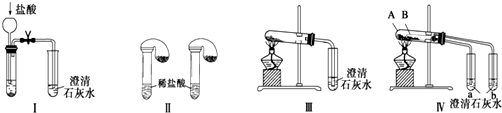
| A. | 根据图Ⅰ所示实验,可以根据澄清石灰水是否变浑浊鉴别碳酸钠和碳酸氢钠固体 | |
| B. | 在图Ⅱ所示实验的左右两只试管中加入足量的盐酸,然后向两个气球中分别加入等物质的量的碳酸钠和碳酸氢钠固体,根据反应后气球的大小可鉴别两种固体 | |
| C. | 与实验Ⅲ相比,实验Ⅳ的突出优点是可以做到用一套装置同时进行两个对比实验,而Ⅲ不行 | |
| D. | 若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则小试管B中装入的固体是碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 观察钠的焰色反应需透过蓝色钴玻璃 | |
| B. | 实验室中的各种碱金属单质均保存在煤油中 | |
| C. | 配制一定物质的量浓度的溶液时容量瓶中有少量水不影响实验 | |
| D. |  为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有图标识 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4L | B. | 8L | C. | 10L | D. | 12L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 mol•L-1 | B. | 0.2mol•L-1 | C. | 2 mol•L-1 | D. | 0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在地壳中的含量:Al>Fe>Na | |
| B. | 均能与盐酸反应,但金属钠与盐酸的反应最剧烈 | |
| C. | 钠、铝均能从FeCl3溶液中置换出铁单质 | |
| D. | 钠、铝均能与NaOH溶液反应,但参加反应的物质种类前者少于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25.5g | B. | 39g | C. | 51g | D. | 106.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com