
【题目】按要求写出下列物质的结构简式:
(1)2,4-二氯甲苯的结构简式为____;
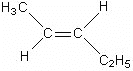
(2)反-2-戊烯的结构简式为___;
(3)分子式为C6H12的某烯烃与氢气加成后得到的烷烃分子中含4个甲基,且该烯烃不存在顺反异构体,则该烯烃的一种结构简式为___。
【答案】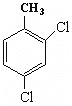
 (CH3)2C=C(CH3)2或CH2=C(CH3)CH(CH3)2或CH2=CHC(CH3)3
(CH3)2C=C(CH3)2或CH2=C(CH3)CH(CH3)2或CH2=CHC(CH3)3
【解析】
⑴先写出甲苯的结构,再从甲苯开始编号,最后书写;
⑵先写2-戊烯的结构简式,再写反-2-戊烯;
⑶先写出有四个甲基的C6H14的结构简式,再根据信息写烯烃,要不存反式异构的。
⑴甲苯为![]() ,2,4-二氯甲苯结构,以甲基为1号位,书写的结构简式为
,2,4-二氯甲苯结构,以甲基为1号位,书写的结构简式为![]() ;
;
故答案为:![]() ;
;
⑵2-戊烯的结构简式CH3CH=CHCH2CH3,反-2-戊烯的结构简式为 ,
,
故答案为: ;
;
⑶分子式为C6H14烷烃分子中含4个甲基,其结构可能为(CH3)2CHCH(CH3)2、CH3CHC(CH3)3,由烯烃加成得到,且该烯烃不存在顺反异构体,可能结构为(CH3)2C=C(CH3)2、CH2=C(CH3)CH(CH3)2、CH2=CHC(CH3)3,
故答案为:(CH3)2C=C(CH3)2或CH2=C(CH3)CH(CH3)2或CH2=CHC(CH3)3;


科目:高中化学 来源: 题型:
【题目】若往![]() 的弱酸
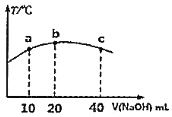
的弱酸![]() 溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是______
溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是______![]() 填序号
填序号![]() 。
。
![]() 该烧碱溶液的浓度为
该烧碱溶液的浓度为![]()
![]() 该烧碱溶液的浓度为
该烧碱溶液的浓度为![]()
![]() 的电离平衡常数:b点
的电离平衡常数:b点![]() 点
点
![]() 从b点到c点,混合溶液中一直存在:
从b点到c点,混合溶液中一直存在:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是重要的基础化工原料,广泛用于制药、染化、塑胶助剂等行业。某兴趣小组模拟PCl3直接氧化法制备POCl3,实验装置设计如下:
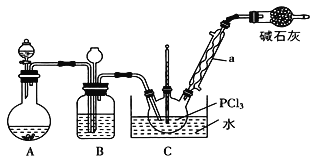
有关物质的部分性质如下表:
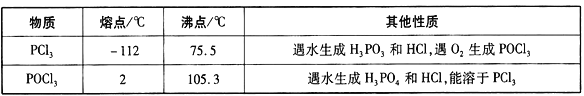
回答下列问题:
(1)仪器a的名称是_____________。装置A中发生反应的化学方程式为_______。
(2)装置C中制备POCl3的化学方程式为________________________________。
(3)C装置控制反应在60~65℃进行,其主要目的是_______________________。
(4)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
I.取xg产品于锥形瓶中,加入足量NaOH溶液,待完全反应后加稀硝酸至溶液显酸性;
II.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀;
III.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
IV.加入指示剂,用c mol·L-1 NH4SCN溶液滴定过量Ag+至终点,记下所用体积为VmL。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是(填序号)________,滴定终点的现象为_____________。
a.酚酞 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②Cl元素的质量分数为(列出算式)________________。
③若取消步骤III,会使步骤IV中增加一个化学反应,该反应的离子方程式为________;该反应使测定结果________(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向浓度均为 0.1mol·L1、体积均为100mL的两种一元酸HA、HB的溶液中,分别加入固体NaOH,溶液中的lg![]() 随加入 NaOH 的物质的量的变化如图所示。下列说法正确的是
随加入 NaOH 的物质的量的变化如图所示。下列说法正确的是

A.由水电离出的 c(H+)的顺序为:c﹥a﹥b
B.b 点时酸碱恰好完全中和
C.c 点溶液中:c(B)﹥c(HB)
D.常温下电离常数:HA﹤HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体数目的叙述中,正确的是( )
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有3种
B.结构简式为![]() 的烃,分子中含有两个苯环的该烃的同分异构体为2种
的烃,分子中含有两个苯环的该烃的同分异构体为2种
C.含有5个碳原子的饱和链烃,其一氯取代物有8种
D.菲的结构简式为 ,它与硝酸反应,可生成3种一硝基取代物
,它与硝酸反应,可生成3种一硝基取代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A. 甲烷的燃烧热为 890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ/mol
B. 500℃、30MPa 下,将 0.5mol N2和 1.5molH2置于密闭容器中充分反应生成 NH3(g),放热 19.3 kJ,其热化学方程式为:N2(g)+3H2(g) ![]() 2NH3(g) △H = -38.6 kJ/mol
2NH3(g) △H = -38.6 kJ/mol
C. 稀盐酸和 稀氢氧化钠溶液混合, 其热化学方程式为:H+(aq)+OH-(aq)=H2O(1) △H = -57.3 kJ/mol
D. 1molH2完全燃烧放热 142.9kJ,则氢气燃烧的热化学方程式为: 2H2(g)+O2(g)=2H2O(1)△H =+285.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
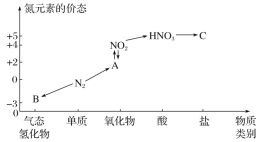
(1)写出 N2 的一种用途: ________________。
(2)B 物质的电子式为: ________________。
(3)HNO3与图中的物质 C 常用于检验 Cl-的存在,则 C 的化学式为______________。
(4)实验室制取物质 B 的化学方程式为 ______________。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为 ___________。
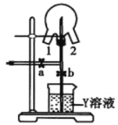
(6)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口 1 通入氨气,然后关闭 b 活塞,再通过瓶口 2 通入氯气。
①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为________,请设计一个实验方案鉴定该固体中的阳离子____________
② 实验完毕后,观察到三颈瓶内还有黄绿色气体, 简述如何处理才能不污染环境___________________。
(7)将 3.2g 铜与 60.0mL 一定浓度的硝酸发生反应,铜完全溶解,产生 NO2 和 NO 混合气体的体积为 8.96L(标况)。待产生的气体全部释放后,向溶液加入 100mL 2.0mol/L 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 _______________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HA的酸性弱于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1 molL-1的HA溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的 物质的量浓度的负对数与溶液的pH的变化悄况如图所示。

下列说法正确的是( )
A. 曲线Ⅰ表示溶液的pH与-lgc(A-)的变化关系
B. ![]()
C. 溶液中水的电离程度:M>N
D. N点对应的溶液中c(Na+)>Q点对应的溶液中c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.不存在活化能为0的反应
B.对于反应COCl2(g)![]() CO(g)+Cl2(g)ΔH > 0,降低温度,正反应速率增大,逆反应速率减小
CO(g)+Cl2(g)ΔH > 0,降低温度,正反应速率增大,逆反应速率减小
C.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增加
D.加入适宜的催化剂,能改变反应历程,降低反应的活化能,增大平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com