
下列说法错误的是()
A. 食物放在冰箱中会减慢食物变质的速率
B. 钾的金属性强,所以钾与水的反应比钠的反应剧烈
C. 2 mol SO2与1 mol O2混合后充分反应生成2 mol SO3
D. 面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸
考点: 化学反应的可逆性;化学反应速率的影响因素;碱金属的性质.
专题: 化学平衡专题;化学反应速率专题.
分析: A.降温,化学反应速率减慢;
B.钾的金属性强,所以钾比钠活泼;
C.根据反应的可逆性的特点判断;
D.表面积越大,反应速率越快.
解答: 解:A.降温,化学反应速率减慢,故食物放在冰箱中会减慢食物变质的速率,故A正确;
B.钾的金属性强,所以钾比钠活泼,故钾与水的反应比钠的反应剧烈,故B正确;
C.SO2与O2反应生成SO3是可逆反应,反应物不可能100%地全部转化为生成物,故2molSO2与1molO2混合后充分反应生成的SO3小于2mol,故C错误;
D.面粉的主要营养素淀粉是可以燃烧的,表面积越大,反应速率越快,故D正确,
故选C.
点评: 本题考查反应速率的影响因素、碱金属的活泼性、可逆反应的特点,难度不大.要注意平时知识的积累.


科目:高中化学 来源: 题型:
实验室用KMnO4与密度为1.19g•cm﹣3,溶质质量分数为36.5%的HCl溶液反应制取氯气,反应方程式为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)用双线桥法分析电子转移的方向和数目(直接在上述方程式中表示).
(2)若反应中有0.5mol电子转移,被氧化的HCl的物质的量是 mol;
(3)c(HCl)= ;
(4)取上述盐酸0.1L与15.8gKMnO4充分反应,生成标况下的Cl2的体积V(Cl2)= L.
查看答案和解析>>
科目:高中化学 来源: 题型:
在某无色透明的酸性溶液中,能共存的离子组是()
A. Na+、K+、SO42﹣、HCO3﹣ B. Cu2+、K+、SO42﹣、NO3﹣
C. Na+、K+、Cl﹣、NO3﹣ D. Fe3+、K+、SO42﹣、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
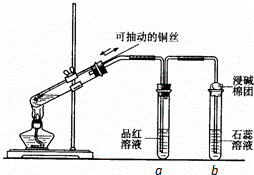
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式: .
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用.
试管a中的现象是 ,作用是 .
试管b中的现象是 ,作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
用足量的铁片与一定量的稀硫酸反应制氢气,下列措施既能使氢气的生成速率加快,又不影响氢气的产量的是()
A. 滴入适量Na2SO4溶液
B. 不用稀硫酸,改用98%的浓硫酸
C. 加入少量碳酸钠固体
D. 不用铁片,改用等质量的铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 等物质的量的氢氧根离子(OH﹣)与甲基(﹣CH3)所含电子数相等
B. 铁、Cu、稀硫酸组成的原电池,当金属铁质量减轻5.6g时,产生H2 2.24L
C. 16g甲烷分子中含有共价键数目共为4NA
D. 2.8g乙烯与丙烯的混合物中含碳原子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃组成的混合气体0.1mol,完全燃烧得到0.16molCO2和3.6g水,下列说法错误的是()
A. 混合气体中一定有甲烷
B. 混合气体中一定是甲烷和乙烷
C. 混合气体中一定没有乙烷
D. 混合气体中一定没有乙炔(C2H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积相同的三个容器里分别充入三种气体①氢气;②二氧化碳;③氧气,并保持三个容器内气体的温度和密度均相等,下列说法正确的是()
A. 分子数目:①=②=③ B. 质量关系:①<③<②
C. 压强关系:①>③>② D. 原子数目:②>③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
氧是地壳中含量最多的元素.
(1)氧元素基态原子核外未成对电子数为 个.
(2)H2O分子内的O﹣H键、分子间的范德华力和氢键从强到弱依次为 . 的沸点比
的沸点比 高,原因是 .
高,原因是 .
(3)H+可与H2O形成H3O+,H3O+原子采用 杂化.H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角大,原因为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com