
| A. | H2O、HCOOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有氧化性,都是氧化性酸 | |
| C. | HF、HClO、NH3都易溶于水,都是电解质 | |
| D. | C2H2、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
分析 A.氧化物由两种元素构成,其中有一种元素为氧元素;
B.HClO、浓H2SO4、HNO3均具有氧化性,都是氧化性酸;
C.电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
D.乙炔不是酸.
解答 解:A.氧化物由两种元素构成,其中有一种元素为氧元素,所以HCOOH、Cu2(OH)2CO3不是氧化物,故A错误;
B.HClO、浓H2SO4、HNO3均具有氧化性,都是氧化性酸,故B正确;
C.氨气在水溶液中与水反应生成一水合氨,一水合氨部分电离出铵根离子和氢氧根离子,氨气自身不能电离,故氨气是非电解质,故C错误;
D.乙炔不是酸,不能电离出氢离子,故D错误;
故选B.
点评 本题考查了物质的分类,涉及氧化物、酸、电解质的判断,难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质.


科目:高中化学 来源: 题型:解答题
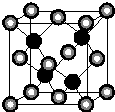 有A、D、E、G、M、L六种前四周期的元素.A元素的单质,是最轻的气体,D原子核外电子有11运动状态,E的负一价离子的核外3p轨道全充满.G原子的2p轨道有2个未成对电子,短周期元素M原子与G原子具有相同的价层电子排布.L位于周期表第12纵行且是六种元素中原子序数最大的.下图是由M、L形成的化合物R,其晶胞结构如图所示.
有A、D、E、G、M、L六种前四周期的元素.A元素的单质,是最轻的气体,D原子核外电子有11运动状态,E的负一价离子的核外3p轨道全充满.G原子的2p轨道有2个未成对电子,短周期元素M原子与G原子具有相同的价层电子排布.L位于周期表第12纵行且是六种元素中原子序数最大的.下图是由M、L形成的化合物R,其晶胞结构如图所示.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用铂作催化剂 | B. | 降低温度 | ||
| C. | 缩小体积增大压强 | D. | 增大接触面积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1mol•L-1 氯化钠溶液 | B. | 75mL 1mol•L-1 氯化钙溶液 | ||
| C. | 150mL 3mol•L-1 氯化钾溶液 | D. | 75mL 2mol•L-1 氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
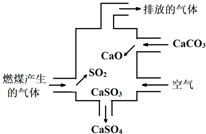
| A. | 使用此装置可减少导致酸雨的气体形成 | |
| B. | 用酸性高锰酸钾溶液检验废气处理是否达标 | |
| C. | 整个过程的总反应可表示为:2SO2+2CaCO3+O2=2CaSO4+2CO2 | |
| D. | 排放的气体是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+和Fe2+ | B. | Al3+和Na+ | C. | Fe2+和NH4+ | D. | Fe3+和Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
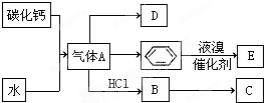
 ;D的空间构型为平面结构,键角为120°;
;D的空间构型为平面结构,键角为120°; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应.
+HBr,其反应类型为取代反应. ,其反应类型为加聚反应.
,其反应类型为加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11:1 | B. | 10:1 | C. | 9:1 | D. | 1:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com