
【题目】在如图中,甲烧杯中盛有100mL 0.50molL﹣1 AgNO3溶液,乙烧杯中盛有100mL 0.25molL﹣1CuCl2溶液,A,B,C,D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则 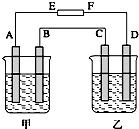
(1)电源E为极,F为极.
(2)A极的电极反应式为 , 析出物质mol.
(3)B极的电极反应式为 , 析出气体mL(标).
(4)C极的电极反应式为 , 析出的物质mol.
(5)D极的电极反应式为 , 析出气体mL(标况).
(6)甲烧杯中滴入石蕊试液,极附近变红,若继续电离,在甲烧杯中最终得到溶液.
【答案】
(1)负;正
(2)Ag++e﹣=Ag;0.025
(3)4OH﹣﹣4e﹣═H2O+O2↑;140
(4)Cu2++2e﹣=Cu;0.0125mol
(5)2Cl﹣﹣2e﹣=Cl2↑;280
(6)B;硝酸
【解析】解:(1)电解池中,发现A极比C极重1.9g,则A极是阴极,和电源的负极相连的是阴极,即E是负极,F是正极,B是阳极,C是阴极,D是阳极,所以答案是:负;正;(2)A极是阴极,电极反应式为:Ag++e﹣=Ag,C是阴极,电极反应为:Cu2++2e﹣=Cu,析出金属铜,A极比C极重1.9g,设电路转移电子是x,则108x﹣32x=1.9,所以x=0.025mol,析出金属银的物质的量是0.025mol,所以答案是:Ag++e﹣=Ag;0.025mol;(3)B是阳极,该极上是氢氧根离子失电子,电极反应为:4OH﹣﹣4e﹣═H2O+O2↑,电路转移电子0.025mol,生成氧气是0.00625mol,体积是0.00625mol×22.4L/mol=0.14L=140mL,所以答案是:4OH﹣﹣4e﹣═H2O+O2↑;140;(4)C是阴极,电极反应式为:Cu2++2e﹣=Cu,电路转移电子0.025mol,生成金属铜是0.0125mol,所以答案是:;0.0125mol;(5)D是阳极,该极上的电极反应是:2Cl﹣﹣2e﹣=Cl2↑,电路转移电子0.025mol,生成氯气是0.0125mol,体积是280mL,所以答案是:2Cl﹣﹣2e﹣=Cl2↑;280;(6)电解硝酸银,在阴极上是Ag++e﹣=Ag,阳极B上是:4OH﹣﹣4e﹣═H2O+O2↑,B电极附近产生硝酸,滴入石蕊试液,显示红色,所以答案是:B;硝酸.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】NaHCO3 和 NaHSO4 溶液混合后,实际参加反应的离子是( )
A.CO32﹣ 和 H+B.HCO3﹣ 和HSO4﹣
C.CO32﹣ 和HSO4﹣D.HCO3﹣ 和 H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示: 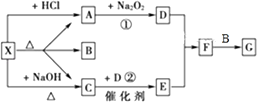
图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
(1)物质X可以是 , C是 , F是 .
(2)反应①的化学方程式是 , 反应②的化学方程式是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为了制取氨气和探究氨气的有关性质,进行了下列实验. 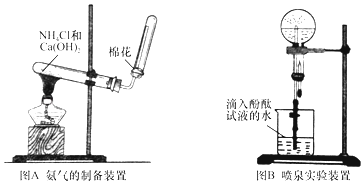
(1)根据图A写出实验室制取氨气的化学方程式;
(2)收集氨时,试管口棉花的作用;验满的方法是;收集干燥的氨时,使用的干燥剂是;
(3)实验室制取下列气体时,与实验室制取氨气的气体发生装置相同的是 .
A.氢气
B.氧气
C.氯气
D.二氧化碳
(4)图B装置进行喷泉实验,烧瓶中充满氨气,引发水上喷的操作是;所得溶液呈性(填酸性、碱性或中性),解释原因(用化学方程式表示) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系甲 ![]() 乙
乙 ![]() 丙,下列有关物质的推断不正确的是( )
丙,下列有关物质的推断不正确的是( )
A.若甲为焦炭,则丁可能是O2
B.若甲为AlCl3 , 则丁可能是浓氨水
C.若甲为SO2 , 则丁可能是氨水
D.若甲为NaOH 溶液,则丁可能是H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3 , 不考虑其他杂质)制取七水合硫酸亚铁(FeSO47H2O),设计了如图流程:下列说法不正确的是( ) 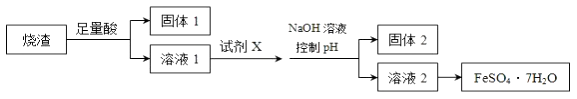
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO2 , 控制pH为使Al3+转化为Al(OH)3 , 进入固体2
C.从溶液2得到FeSO47H2O产品的过程中,须控制条件防止其氧化
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO47H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铜矿主要含Cu2(OH)2CO3 , 还含少量Fe、Si的化合物.实验室以此铜矿石为原料制备CuSO45H2O及CaCO3 , 部分步骤如图: 
请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有(填离子符号);验证所含离子所用的试剂是在 .
(2)可用生成的CO2制取优质碳酸钙.制备时,先向氯化钙溶液中通入氨气,再通入CO2 .
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气.某学习小组选取图1所给部分装置制取并收集纯净的氨气.
如果按气流方向连接各仪器接口,你认为正确的顺序为a→、→、→i.
其中与i相连漏斗的作用是 .
②为探究氨气和氯气的反应(图2)
a.装置A、B,B装置内的药品依次是、 .
b.装置C可用于探究氯气与氨气(已知氯气和氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应.实验打开开关1、3,关闭2,先向烧瓶中通入 , 然后关闭1、3,打开2,向烧瓶中缓缓通入一定量的另一种气体.实验一段时间后向烧瓶内出现浓厚的白烟并在容器内壁凝结.
(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:
a.将1.25g铜矿石制取的CuSO45H2O于锥形瓶中,加入适量水完全溶解;
b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;
c.过滤;
d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸.则铜矿石中Cu2(OH)2CO3质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀土元素R的精矿样品中,R的氧化物的质量分数为0.8515.20.2g该样品与100mL 1mol/L稀硫酸恰好完全反应(杂质不反应),生成ROSO4和H2O,则R的相对原子质量约为( )
A.78
B.140
C.156
D.172
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com