
| A. | 高分子分离膜应用于食品工业中,可用来浓缩天然果汁、乳制品加工、酿造业等 | |
| B. | 复合材料一般是以一种材料做基体,另一种材料作为增强剂 | |
| C. | 合成高分子材料制成的人工器官一般都受到人体的排斥,难以达到生物相容的程度 | |
| D. | 导电塑料是应用于电子工业的一种新型有机高分子材料 |
分析 A.高分子分离膜是由聚合物或高分子复合材料制得的具有分离流体混合物功能的薄膜;
B.复合材料是由两种或两种以上不同性质的材料,通过物理或化学的方法,在宏观上组成具有新性能的材料;
C.医用高分子材料归属于功能高分子材料;
D.导电塑料是将树脂和导电物质混合,用塑料的加工方式进行加工的功能型高分子材料.
解答 解:A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿造业等,故A正确;
B.复合材料是由两种或两种以上不同性质的材料,通过物理或化学的方法,在宏观上组成具有新性能的材料,一般是以一种材料作为基体,另一种材料作为增强剂,故B正确;
C.医用高分子材料归属于功能高分子材料,它们都无毒、具有良好的生物相容性和稳定性,有足够的机械强度等特点,故C错误;
D.导电塑料是将树脂和导电物质混合,用塑料的加工方式进行加工的功能型高分子材料.主要应用于电子、集成电路包装、电磁波屏蔽等领域,故D正确;
故选C.
点评 本题考查了高分子化合物的结构与性质、合成材料的应用,题目难度中等,明确常见材料的组成、分类及及用途为解答关键,试题培养了学生灵活应用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:解答题
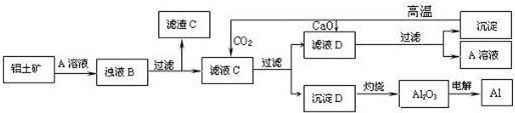
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
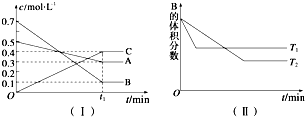
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸为电解质溶液 | B. | 锌为原电池正极 | ||
| C. | 铁极质量不变 | D. | 铜为原电池正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
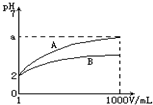 pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )| A. | A、B溶液浓度一定相等 | B. | 稀释后A溶液酸性比B溶液强 | ||
| C. | a=5时,A是强酸,B是弱酸 | D. | 若A、B都是弱酸,则2<a=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
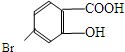 ,它的含氧官能团名称为羧基、羟基.
,它的含氧官能团名称为羧基、羟基.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
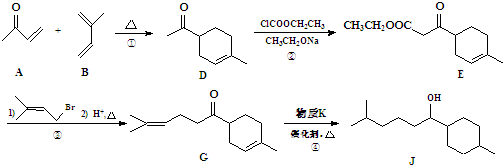
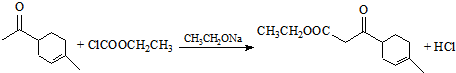
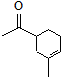 .
.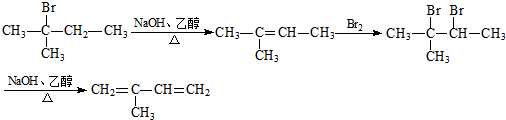 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 酸 | 碱 | 盐 | 氧化物 | |
| A | 硫 酸 | 纯 碱 | 硫酸钡 | 水 |
| B | 氢硫酸 | 烧 碱 | 纯 碱 | 石灰石 |
| C | 碳 酸 | 熟石灰 | 小苏打 | 二氧化硫 |
| D | 二氧化碳 | 苛性钾 | 食 盐 | 石灰石 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com