
【题目】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:

(1)装置A的分液漏斗中盛装的试剂是___________,烧瓶中加入的试剂是___________
发生的离子反应方程式________________;
(2)虚线框内是一个装有未知试剂的广口瓶,该试剂是___________,说明装置的作用________________;
(3)装置B中盛放的试剂是______________(选填下列所给试剂的字母),实验现象为___________________,化学反应方程式是__________________________________;
A.Na2S溶液 B.Na2SO3 溶液 C.Na2SO4 溶液
(4)已知:①硫酸比次氯酸稳定;②高氯酸比硫酸酸性强;③S2- 比Cl- 易被氧化;④HCl比H2S稳定;⑤铜与盐酸不反应,但能与浓硫酸反应;⑥铁与氯气加热生成三氯化铁,铁与硫加热生成硫化亚铁。可说明氯比硫非金属性强的是_______;
A.全部 B.②③④⑥ C.①②④⑤⑥ D.除①以外
(5)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,且生成物中ClO-和ClO3-的物质的量浓度之比为5∶1,请写出离子反应方程式________________________________。
【答案】浓HCl MnO2 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 饱和食盐水 除去Cl2中混有的HCl A 有黄色沉淀生成 Cl2+S2-=S↓+2Cl- B 8Cl2+16OH-=10Cl-+5ClO-+ClO3-+8H2O
Mn2++Cl2↑+2H2O 饱和食盐水 除去Cl2中混有的HCl A 有黄色沉淀生成 Cl2+S2-=S↓+2Cl- B 8Cl2+16OH-=10Cl-+5ClO-+ClO3-+8H2O
【解析】
(1)根据实验的目的可知要先获得氯气,需制取氯气的装置,进而确定装置中的物质和反应的原理方程式;
(2)二氧化锰和浓盐酸反应制得的氯气中含有氯化氢杂质,可以用饱和食盐水除去;
(3)证明氯气的氧化性强于硫单质的实验室氯气和硫化钠之间的反应,氧化性越强则原子的得电子能力强;
(4)判断原子的得电子能力强弱的方法:最高价氧化物对应水化物的酸的酸性强弱、离子的还原性强弱、氢化物的稳定性、将同样的金属氧化到的价态等;
(5)用氢氧化钠对氯气进行尾气处理.分别写出氯气与NaOH溶液反应的方程式,ClO-和ClO3-的物质的量浓度之比为5∶1,按比例写出总反应。
根据题意,验证氯元素的非金属性比硫元素的非金属性强的原理是氯气可以将硫从其化合物硫钠中置换出来.
(1)装置A的作用是制取氯气,分液漏斗中盛装的试剂是浓盐酸,烧瓶中加入的试剂是MnO2,发生的离子反应方程式:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)二氧化锰和浓盐酸反应制得的氯气中含有氯化氢杂质,可以用盛有饱和食盐水的洗气瓶将其除去,虚线框内的实验装置图为: ,
,
(3)氯气可以将硫从其化合物中置换出来的事实可以证明氯元素的非金属性比硫元素的非金属性强,故选A;反应的原理是:S2-+Cl2=2Cl-+S↓,有淡黄色沉淀生成;
(4)最高价氧化物对应水化物的酸的酸性越强,则原子的得电子能力越强,故②正确,S2-比Cl-易被氧化,说明单质的氧化性是氯气强于硫,所以原子的得电子能力Cl强于S,故③正确,元素的氢化物的稳定性越强则原子的得电子能力越强,故④正确,单质将同样的金属氧化到的价态越高则原子的得电子能力强,故⑥正确,硫原子与氯原子电子层数相同,同周期元素的原子半径越小,得电子能力越强,故⑦正确,
故选B;
(5)用氢氧化钠对氯气进行尾气处理.ClO-和ClO3-的物质的量浓度之比为5∶1,分别写出氯气与NaOH溶液反应生成ClO-和ClO3-的方程式,①Cl2+2OH-═Cl-+ClO-+H2O,和②3Cl2+6OH-═5Cl-+ClO3-+3H2O,按比例写出总反应①×5+②得:8Cl2+16OH-=10Cl-+5ClO-+ClO3-+8H2O。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】向一定量下列物质的溶液中逐滴加入氢氧化钠溶液,先生成白色沉淀,后沉淀逐渐溶解,这种物质是( )
A.硫酸镁B.四羟基合铝酸钠C.氯化铝D.氯化铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 充电电池不能无限制地反复充电、放电
B. 燃料电池是一种高效且对环境友好的新型电池
C. 化学电池的反应原理是自发的氧化还原反应
D. 铅蓄电池和锌锰干电池都是可充电电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,能说明氯的非金属性比硫强的是( )
①HClO的氧化性比H2SO4的氧化性强 ②常温下氯气是气态而硫是固态
③盐酸酸性比氢硫酸强 ④HCl比H2S稳定 ⑤H2S能被Cl2氧化成硫
⑥SCl2分子中氯显-1价 ⑦氯气与氢气化合比硫与氢气化合要容易进行
⑧Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
A. ①②③④⑤⑥⑦⑧ B. ①④⑤⑥⑦
C. ④⑤⑥⑦⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出11种元素在周期表中的位置,按要求回答下列各题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑧ | ||||||
3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
4 | ② | ④ | ⑩ |
(1)这11种元素中,化学性质最不活泼的元素是______(填元素符号,下同),失电子能力最强的原子是______,得电子能力最强的单质与水反应的化学方程式是______________,常温下单质为液态的非金属单质是____________;
(2)⑦⑧⑨气氢化物的稳定性:________>________>________
(3)写出③的单质置换出⑥的单质的化学方程式:__________________;
①和⑤两种元素最高价氧化物对应的水化物相互反应的化学方程式为_____________;
⑨的最高价氧化物对应水化物的水溶液与⑤的最高价氧化物反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池放电时的反应:PbO2+Pb+2H2SO4═2PbSO4+2H2O,下列有关放电时的说法正确的是( )
A. 负极的电极反应式是:Pb+SO42﹣﹣2e﹣═PbSO4
B. PbO2作正极,电极发生氧化反应
C. 当转移的电子数为3.01×1023时,参与反应的Pb的质量为103.5 g
D. 溶液中H+移向负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
①铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线拧在一起
②汽车尾气中含有能污染空气的氮氧化物,主要是汽油燃烧不充分造成的
③从海水中提取物质都必须通过化学反应才能实现
④“辽宁舰”上用于舰载机降落拦阻索的特种钢缆属于新型无机非金属材料
⑤明矾可以用于净水,主要是由于Al3+水解生成的少量氢氧化铝胶体有净水作用
A.②③⑤ B.①②④ C.①③④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“茶倍健"牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下所示。下列关于EGC的叙述中不正确的是

A. 1molEGC与4molNaOH恰好完全反应
B. 分子中所有的原子不可能共平面
C. 易发生氧化反应和取代反应,难发生加成反应
D. 遇FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通电条件下,用如图所示装置由乙二醛(OHC-CHO)制备乙二酸(H00C-COOH)。其制备反应为:OHC-CHO+2Cl2+2H2O→HOOC-COOH+4HCl。下列说法正确的是
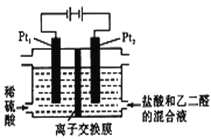
A. 每消耗0.1mol乙二醛在Pt1极放出2.24L气体(标准状况)
B. Pt1的电极反应为:4OH--4e-=2H2O+O2↑
C. 盐酸是起提供Cl-和增强导电性的作用
D. 每得到lmol乙二酸将有2molH+从右室迁移到左室
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com