
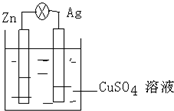
 (1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.
(1)在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是氧化反应(“氧化”或“还原”).电极反应式为Zn-2e-═Zn2+.科目:高中化学 来源: 题型:选择题
| A. | Fe3O4(Al2O3) | B. | KCl(NaCl) | C. | SiO2(CaCO3) | D. | FeCl2溶液(FeCl3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第15列元素的最高价氧化物的化学式为R2O5 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | L层电子数为奇数的所有元素所在族的序数与元素原子L层电子数相等 | |
| D. | M层电子数为奇数的所有元素所在族的序数与元素原子M层电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | σ键比π键的电子云重叠程度大,形成的共价键强 | |
| B. | 碳碳双键的键能是碳碳单键键能的2倍 | |
| C. | s-s σ键与s-p σ键的电子云形状对称性相同 | |
| D. | N2分子中有一个σ键,2个π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
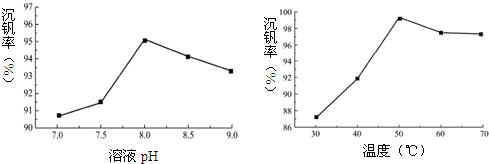
| 实验步骤与结论: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na同主族,因为Na在空气中加热生成Na2O2,所以Li在空气中加热生成Li2O2 | |
| B. | F、Cl同主族,因为HCl是强酸,所以HF也是强酸 | |
| C. | Li、Na同主族,因为Na保存在煤油中,所以Li也保存在煤油中 | |
| D. | F、Cl同主族,因为Cl2也是有色气体,所以F2也是有色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
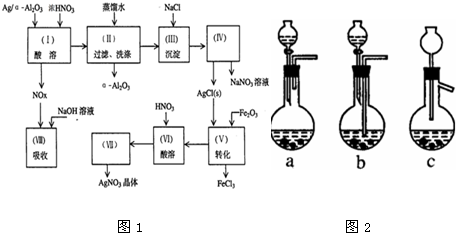
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ;
; .
. ;
; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com