

分析 研究二氧化硫催化氧化的过程(加热装置已省略),并制取少量三氧化硫晶体:A装置:制取二氧化硫,B装置:制取氧气,C装置:干燥二氧化硫和氧气;使二氧化硫和氧气混合均匀;通过观察气泡控制气体比例和流速,D装置:D中发生的是SO2催化氧化的反应,E装置:E的作用是冷却装置,使SO3凝结成固体与SO2分离,F装置:高锰酸钾溶液氧化二氧化硫,G装置:尾气处理.
(1)该实验主要是气体间的反应,所以实验前,必须进行的操作是检查装置的气密性;
(2)D中发生的是SO2催化氧化的反应,即二氧化硫与氧气催化氧化生成三氧化硫;
(3)C装置中盛放的液体药品是浓硫酸,装置C作用:干燥二氧化硫和氧气;使二氧化硫和氧气混合均匀;通过观察气泡控制气体比例和流速;
(4)装置E的作用是冷却装置,三氧化硫的沸点较低,通过冰水混合物,使SO3凝结成固体与SO2分离,装置F中高锰酸钾溶液会和二氧化硫反应逐渐褪色,生成Mn2+,二氧化硫被氧化为硫酸,根据化合价升降总数相等以及电荷守恒书写离子反应方程式;
(5)若装置F中有40mL 2.5mol•L-1NaOH溶液,反应后增重4.8g,吸收的为二氧化硫气体,依据反应方程式及二氧化硫氢氧化钠物质的量进行分析判断生成产物,然后写出反应的化学方程式即可.
解答 解:(1)该实验的目的是研究二氧化硫催化氧化的过程,二氧化硫为气体,参加反应的氧气为气体,主要是气体间的反应,为了保证实验顺利进行,需在实验前必须进行的操作是检查装置的气密性,
故答案为:检查装置的气密性;
(2)D中发生的是SO2与氧气催化氧化生成三氧化硫,化学方程式为:2SO2+O2$?_{△}^{催化剂}$2SO3,
故答案为;2SO2+O2$?_{△}^{催化剂}$2SO3;
(3)探究二氧化硫催化氧化的过程,需对二氧化硫、氧气进行干燥,C装置中盛放的液体药品是浓硫酸,C装置除了干燥作用,还能使二氧化硫和氧气混合均匀;通过观察气泡控制气体比例和流速,
故答案为:干燥二氧化硫和氧气;使二氧化硫和氧气混合均匀;通过观察控制气体比例和气流速度;
(4)装置E的作用是冷却装置,三氧化硫的沸点较低,通过冰水混合物,使SO3凝结成固体与SO2分离,装置F中高锰酸钾溶液会和二氧化硫反应逐渐褪色,生成Mn2+,二氧化硫被氧化为硫酸,S:+4→+6,↑2,×5,Mn:+7→+2,↓5,×2,所以反应的离子方程式为:5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+,
故答案为:使SO3凝结成固体与SO2分离;5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+;
(5)若n(SO2):n(NaOH)=1:2反应按照反应:SO2+2NaOH═Na2SO3+H2O;若n(SO2):n(NaOH)=1:1,反应按照反应SO2+NaOH═NaHSO3;装置Ⅳ中有40mL 2.5mol•L-1 NaOH溶液中n(NaOH)=0.1mol,n(SO2)=$\frac{4.8g}{64g/mol}$=0.075mol;n(SO2):n(NaOH)=0.075:0.1=3:4,所以生成产物为亚硫酸钠和亚硫酸氢钠,
设生成亚硫酸钠xmol、亚硫酸氢钠ymol,
则:$\left\{\begin{array}{l}{x+y=0.075}\\{2x+y=0.1}\end{array}\right.$,解得:$\left\{\begin{array}{l}{x=0.025}\\{y=0.05}\end{array}\right.$,
即n(Na2SO3):n(NaHSO3)=1:2,
所以反应的化学方程式为:3SO2+4NaOH═Na2SO3+2NaHSO3+H2O,
故答案为:3SO2+4NaOH═Na2SO3+2NaHSO3+H2O.
点评 本题主要考查工业接触法制硫酸的原理,侧重于学生的分析能力和实验能力的考查,为高考常见题型,重点考查制备过程中的注意问题和条件的选择依据,注重了对知识的综合运用和迁移能力考查,题目难度中等.


科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:推断题
有机物G是一种“β-兴奋剂”,其合成路线如下:

已知:

(1)写出化合物E同时符合下列条件的所有同分异构体有 种。
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基
②1H-NMR谱显示分子中含有苯环,且苯环上只有一种不同化学环境的氢原子。
③苯环上只有4个取代基,能发生银镜反应
(2)下列说法不正确的是
A.化合物B生成C的反应为取代反应
B.1mol化合物D最多与4molH2发生加成反应
C.化合物D生成E的条件为浓氯水/铁屑
D.化合物G的分子式为C17H14Cl2NO3
(3)写出E+F→G的化学方程式 。
(4)根据题中信息,设计以苯和CH3COCl为原料制备F的合成路线(用流程图表示,其他无机试剂任选)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期月考一化学试卷(解析版) 题型:选择题
化学在绿色发展、循环发展、低碳发展及推进生态文明建设中正发挥着积极作用,一卜列做法与可持续发展宗旨相违背的是
A.加大清洁能源的开发利用,提高资源的利用率
B.推广碳捕集和储存技术,逐步实现二氧化碳零排放
C.加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求
D.对工业废水、生活污水净化处理,减少污染物的排放
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
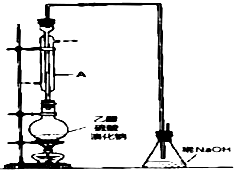 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸、浓硫酸共热发生反应,该反应的化学方程式是CH3CH2OH+HBr$→_{△}^{浓硫酸}$CH3CH2Br+H2O
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃.制备溴乙烷的一种方法是乙醇与氢溴酸、浓硫酸共热发生反应,该反应的化学方程式是CH3CH2OH+HBr$→_{△}^{浓硫酸}$CH3CH2Br+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 相对分 子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| 冬青油 | 152 | 1.180 | 222.2 | 微溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com