
| A. | 地下钢管连接镁块 | B. | 金属护栏表面涂漆 | ||
| C. | 汽车底盘喷涂高分子膜 | D. | 水中的钢闸门连接电源的负极 |
分析 金属防腐的措施中,使用牺牲阳极的阴极保护法,说明该装置构成原电池,被保护的金属作正极,据此分析解答.
解答 解:金属防腐的措施中,使用牺牲阳极的阴极保护法,说明该装置构成原电池,被保护的金属作正极,
A.地下钢管连接镁块,Fe、Mg、电解质溶液构成原电池,Fe失电子能力小于Mg而作正极被保护,所以该保护方法属于牺牲阳极的阴极保护法,故A正确;
B.金属护拦表面涂漆,阻止Fe与空气、水接触,从而防止金属被腐蚀,属于物理方法,故B错误;
C.汽车底盘喷涂高分子膜,阻止Fe与空气、水接触,从而防止金属被腐蚀,属于物理方法,故C错误
D.水中的钢闸门连接电源的负极,是做了电解池的阴极,是外加电源的阴极保护法,故D错误;
故选D.
点评 本题考查了金属的腐蚀与防护,侧重考查基础知识与基本能力,明确原电池原理即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略).已知:
已知A、B、C、D、E均为中学化学中常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略).已知:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
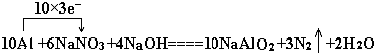
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
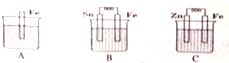
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤ | B. | ②③④⑤ | C. | ②⑤⑥⑦ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 物质的量是度量物质所含微观粒子多少的物理量 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | 等质量的O2和O3中所含氧原子个数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 观察比较外观形态 | B. | 用手触摸比较 | ||
| C. | 放到嘴里品尝一下 | D. | 用化学方法进行鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  | 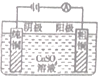 |  | |
| 化工 | 氯碱工业 | 高炉炼铁 | 铜的精炼 | 生产漂白粉 |
| 原理 | 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$ 2NaOH+Cl2↑+ H2↑ | 3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | 阴极: Cu2++2e-═Cu | 2NaOH+Cl2═NaCl+NaClO+H2O |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
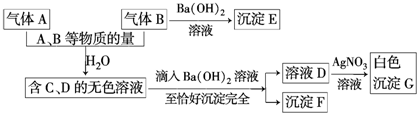
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com