
| A. | 键能:HBr>HCl | B. | 键长:HBr>HCl | ||
| C. | 沸点:HBr>HCl | D. | 共用电子对偏向:HCl>HBr |
分析 A.非金属性越强,共价键的键能越大;
B.原子半径越小,键长越短;
C.相对分子质量越大,沸点越高;
D.元素的非金属性越强,吸引电子能力越强.
解答 解:A.非金属性越强,共价键的键能越大,非金属性:Cl>Br,则键能:HCl>HBr,故A错误;
B.原子半径越小,键长越短,原子半径:Br>Cl,所以键长HBr>HCl,故B正确;
C.相对分子质量越大,沸点越高,相对分子质量:HBr>HCl,则沸点:HBr>HCl,故C正确;
D.元素的非金属性越强,吸引电子能力越强,非金属性:Cl>Br,共用电子对偏向:HCl>HBr,故D正确.
故选A.
点评 本题考查了元素周期律,题目难度不大,注意把握同主族元素性质的递变规律,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:选择题
| A. | pH=2 的HA溶液与pH=12的MOH溶液等体积混合:c(H+)=c(OH-) | |
| B. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) | |
| D. | 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗盐提纯时,为了加快过滤速率,可以用玻璃棒进行搅拌 | |
| B. | 分液操作中,将下层液体放入烧杯中,再将上层液体继续放入另一烧杯中 | |
| C. | 测定硫酸铜晶体结晶水含量时,加热后的坩埚须在干燥器中冷却,再称量 | |
| D. | 蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶瓶壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
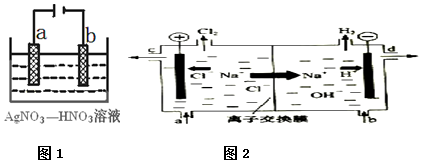
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A-x | B. | A+n-x | C. | A-n-x | D. | A+n+x |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
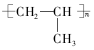 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 | B. | 1 | C. | 0.25 | D. | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com