
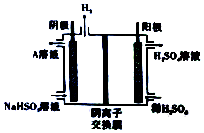
| A. | A溶液为Na2SO4溶液 | |
| B. | 阴极区消耗1molNaHSO3时,同时生成1molA | |
| C. | 当阴极上生成标准状况下1.12LH2时,阳极区溶液pH值降低1 | |
| D. | 阳极电极反应式为HSO3-+H2O-2e-=SO42-+3H+ |
分析 用惰性电极电解NaHSO3溶液,阴极上氢离子放电生成氢气,生成的氢氧根离子和亚硫酸氢根离子发生反应OH-+HSO3-=SO32-+H2O,所以A溶液为Na2SO3,HSO3-通过阴离子交换膜向阳极移动,阳极上HSO3-失电子生成SO42-,结合电子守恒分析.
解答 解:A.用惰性电极电解NaHSO3溶液,阴极上氢离子放电生成氢气,生成的氢氧根离子和亚硫酸氢根离子发生反应OH-+HSO3-=SO32-+H2O,所以A溶液为Na2SO3,故A错误;
B.阴极上2H2O+2e-=H2↑+2OH-,氢氧根离子和亚硫酸氢根离子发生反应OH-+HSO3-=SO32-+H2O,同时,部分HSO3-通过阴离子交换膜向阳极移动,阳极上HSO3-失电子生成SO42-,则阴极区消耗1molNaHSO3时,只有部分转化为Na2SO3,故B错误;
C.当阴极上生成标准状况下1.12LH2时,即0.05mol,则转移电子为0.1mol,阳极电极反应式为HSO3-+H2O-2e-=SO42-+3H+,阳极区生成氢离子为0.15mol,溶液的体积不知道,无法计算氢离子浓度,所以pH变化无法判断,故C错误;
D.HSO3-通过阴离子交换膜向阳极移动,阳极上HSO3-失电子生成SO42-,阳极电极反应式为HSO3-+H2O-2e-=SO42-+3H+,故D正确.
故选D.
点评 本题考查了电解原理,明确发生的电极反应及电子守恒是解答本题的关键,题目难度中等,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: +Br2$\stackrel{FBr_{3}}{→}$ +Br2$\stackrel{FBr_{3}}{→}$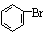 +HBr +HBr | |
| D. | 将CO2通入苯酚钠溶液:2 +CO2+H2O→2 +CO2+H2O→2 +Na2CO3 +Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为负极 | |
| B. | 正极反应为:2O2+4H2O+8e-═8OH- | |
| C. | 燃料电池工作时,溶液中的OH-向正极移动 | |
| D. | 该电池使用一段时间后溶液中KOH的浓度将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与水反应(乙醇) | |
| B. | 乙烯与氯气反应(二氯乙烷) | |
| C. | 液溴与苯用溴化铁作催化剂反应(溴苯) | |
| D. | 等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
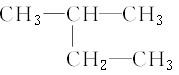 ③金刚石 ④35Cl ⑤
③金刚石 ④35Cl ⑤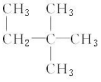
 ⑦
⑦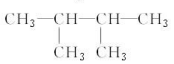 ⑧氯气 ⑨石墨 ⑩37Cl
⑧氯气 ⑨石墨 ⑩37Cl
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClCH2CH2OH | B. | OHC-O-CH2Cl | C. | ClCH2CHO | D. | HOCH2CH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1g乙炔溶于12g苯,所得混合物中含有的碳原子数为NA | |
| B. | 1 mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒 | |
| C. | 标况下,11.2 L的HF所含分子数为0.5 NA | |
| D. | 133.5 g氯化铝固体中含有NA个铝离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8、7 | B. | 9、4 | C. | 4、9 | D. | 6、10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com