
下列叙述正确的是:
A.固体碘转化为紫红色气体,需吸收能量,因共价键被破坏
B.碳酸氢铵是离子化合物,其受热分解产生氨气不仅破坏离子键还破坏了共价键
C.金属和非金属所形成的化学键均为离子键
D.共价键只存在于共价化合物中
科目:高中化学 来源: 题型:
(2013·上海,22)一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO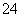 )加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V可能为 ( )
)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO 12.0 g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V可能为 ( )
A.9.0 L B.13.5 L
C.15.7 L D .16.8 L
.16.8 L
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温下,0.05 mol·L-1Fe2(SO4)3溶液中含Fe3+数目小于0.1 NA
B.30g甲醛中含电子对数为4NA
C.12 g石墨烯(单层石墨)中含有六元环的个数是0.5NA
D.室温下,7.1 g氯气与足量石灰乳充分反应转移电子数小于0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于常温下,pH=3的醋酸溶液(I)和 pH=11的氢氧化钠溶液(Ⅱ)的说法正确的是( )
A.I和Ⅱ的物质的量浓度均为0.001mol·L-1
B.将I稀释10倍,溶液中 c(CH3COOH)、 c(OHˉ)均减小
C.I和Ⅱ溶液混合,若c(OH-)>c(H+),则氢氧化钠过量
D.I和Ⅱ等体积混合后,溶液中离子浓度大小为c(CH3COO-)>c(Na+)> c(H+)> c(OH--)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的物质是
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3
A.全部 B.①②③ C.①②③⑤ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器内,可逆反应: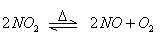 ,达到平衡状态的标志是:
,达到平衡状态的标志是:
(1)单位时间内生成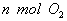 的同时生成
的同时生成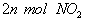
(2)单位时间内生成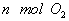 的同时生成
的同时生成
(3)用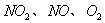 的物质的量浓度变化表示反应速率的比为2:2:1的状态
的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态
A. (1)(3)(4) B. (2)(3)(5)
C. (1)(4)(5) D. (1)(2)(3)(4)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表的位置如下表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法正确的是
| X | Y | ||
| Z | W | Q |
A.钠与Y可能形成Na2Y2化合物
B.Z的最高价含氧酸比X的最高价含氧酸的酸性强
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
Ni、K和F三种元素组成的一个化合物的晶胞如右图所示。该化合物的化学式及Ni的配位数为( )
A.K2NiF4;6 B.K4Ni2F8;8 C.K2NiF3;4 D.K2NiF6;6

查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
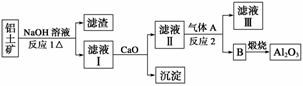
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:

回答下列问题:
(1)写出反应1的化学方程式_______________________________________________。
(2)滤液Ⅰ中加入CaO生成的沉淀是________,反应2的离子方程式为____________。
(3)E可作为建筑材料,化合物C是________,写出由D制备冰晶石的化学方程式________________________________________________________________________。
(4)电解法制铝的化学方程式是________,以石墨为电极,阳极产生的混合气体的成分是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com