
| A. | 铜片作正极 | B. | 正极反应为:2H++2e-═H2↑ | ||
| C. | 溶液中的H+移向正极 | D. | 锌片作负极,锌发生还原反应 |
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA | |
| B. | 80 mL 10 mol/L盐酸与足量 MnO2加热反应,产生Cl2分子数为0.2NA | |
| C. | S2和S8的混合物共6.4 g,其中所含硫原子数一定为 0.2 NA | |
| D. | 含有4 NA个C-C 键的金刚石,其质量为 12 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
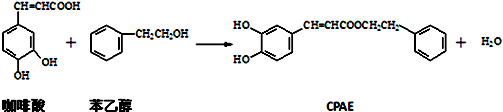
| A. | 1mol CPAE与足量的NaOH溶液、溴水反应,分别最多消耗3mol | |
| B. | 可用金属Na检测上述反应是否残留苯乙醇 | |
| C. | 与苯乙醇互为同分异构体的酚类物质共有9种 | |
| D. | 咖啡酸可发生聚合反应,并且其分子中含有3种含氧官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
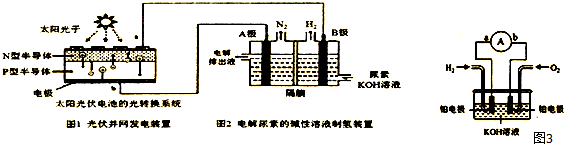
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中的阳离子向正极移动,阴离子向负极移动 | |
| B. | 电流方向是从锌片经导线流向铜片 | |
| C. | 锌片是正极,铜片上有气泡产生 | |
| D. | 电解液的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
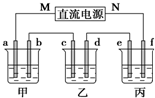 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100毫升的溶液中含有Mg2+、Cl-总数为0.3NA | |
| B. | 100毫升的溶液中含有Mg2+数目是0.1NA | |
| C. | 1升溶液中Mg2+的浓度是0.3mol/L | |
| D. | 1.5升溶液中含有Cl-的浓度是4.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com