
【题目】建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是
A. 钠在氧气中燃烧,钠的氧化产物: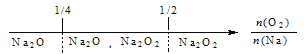
B. 铁在Cl2中燃烧,铁的氧化产物:![]()
C. NH3与Cl2反应,反应产物: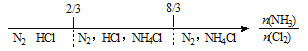
D. FeBr2溶液中通入Cl2,铁元素存在形式: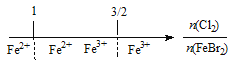
【答案】C
【解析】
试题A.钠在氧气中燃烧,无论相对量的多少,产生的都是Na2O2,错误;B.铁在Cl2中燃烧,无论相对量的多少,产生的都是FeCl3,错误;C.NH3与Cl2反应,当氨气少量时,发生反应:2NH3+3Cl2=6HCl+N2,当氨气过量时发生的总反应是: NH3+3Cl2=6NH4Cl+N2,若介于2:3和8:3之间则产物是NH4Cl、N2、HCl,正确;D.FeBr2溶液中通入Cl2,由于还原性:Fe2+>Br-,首先发生反应:Cl2+2Fe2+=2Fe3++2Cl-,若氯气过量,则发生反应:2Cl2+2Fe2++4Br-=2Fe3++2Cl-+2Br2,所以上述数轴表示不符合反应的先后顺序,错误。


科目:高中化学 来源: 题型:
【题目】隔绝空气加热至500℃时硫酸亚铁铵[(NH4)2Fe(SO4)2]能完全分解,分解产物中含有铁 氧化物、硫氧化物、氨气和水蒸气等。
[实验探究]某化学小组选用下图所示部分装置进行分步实验(夹持装置略)。
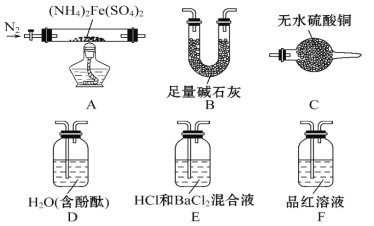
实验Ⅰ 甲同学为探究分解产物中的硫氧化物是 SO2 还是 SO3,连接装置A-E-F-B 进行实验。
(1)实验过程中观察到:E 中没有明显现象,F 中溶液褪色,据此得出的结论是 。
(2)B 的作用是_____。
实验Ⅱ 验证分解产物中含有水蒸气和氨气,并探究残留固体成分。
(3)所选用装置的正确连接顺序为_____(填装置的字母序号)。
(4)证明有水蒸气生成的实验现象为_____。
(5)证明有氨气生成的实验现象为_____。
(6)A 中固体完全分解后变为红棕色粉末,设计实验证明A 中残留固体中含有三价铁_______________。
(7)实验证明(NH4)2Fe(SO4)2 受热分解除上述产物外,还有N2 生成,写出A 中反应的化学方程式__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在新制氯水中滴加NaOH 溶液,溶液中水电离出来的c水(H+)的对数与NaOH 溶液体积之间的关系如图所示。下列推断正确的是

A. 用pH试纸测定E点对应的溶液,其pH=3
B. F、H点对应的溶液中都存在c(Na+)=c(Cl-)+c(ClO-)
C. G点对应的溶液中c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
D. 加水稀释H点对应的溶液,溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:______________ 、________________;
(2)第③步中,生成氢氧化铝的离子方程式是_____________。若往A溶液中通入足量CO2,产生的沉淀为____________________(填化学式);
(3)工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据物质结构和元素周期表的相关知识回答下列问题:
I.用A+、B-、C2-、D表示含有18个电子的离子或分子。请填空:
(1)A元素是__________,B元素是__________,C元素是__________。(用元素符号表示)
(2)物质D由两种元素组成,每个分子中含有三个原子,其分子式是________,电子式是______________。
Ⅱ.X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
(1)Y在元素周期表中的位置为______________,
(2)上述元素的最高价氧化物对应的水化物酸性最强的是______________ (写化学式),非金属气态氢化物还原性最强的是______________(写化学式)。
(3)Y和Z的两元素之间形成的原子个数比为1:1的化合物的电子式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子.在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中不正确的是( )
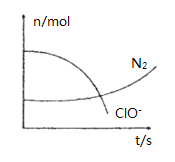
A. 还原剂是含CN-的物质,氧化产物只有N2
B. 氧化剂是ClO-,HCO3-是氧化产物
C. 参与反应的氧化剂与还原剂的物质的量之比为5:2
D. 标准状况下若生成2.24LN2,则转移电子1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16.三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子.有关判断不正确的是( )
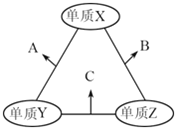
A. X元素位于ⅥA族 B. A不能溶解于B中 C. B的沸点高于C的沸点 D. A和C不可能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物和硫的氧化物是导致酸雨的物质。
(1)SO2有毒,且能形成酸雨,是大气主要污染物之一。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收原理:
①SO2+Ca(OH)2=CaSO3↓+H2O②2CaSO3+O2+4H2O=2(CaSO4·2H2O)碱法的吸收原理:将含SO2的尾气通入足量的烧碱溶液中,请写出对应的化学反应方程式__________;
已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
和石灰-石膏法相比,碱法的优点是吸收快、效率高,缺点是__________;
(2)石灰-石膏法和碱法的基础上,设计了双碱法,能实现物料循环利用。

上述方法中,实现循环利用的物质是__________,请用化学方程式表示在Na2SO3溶液中加入CaO后的反应原理__________。
(3)一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式:____________
(4)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
现有VL某NaOH溶液能完全吸收n mol NO2和m mol NO组成的大气污染物。
①所用烧碱溶液的物质的量浓度至少为________mol·L-1。
②若所得溶液中c(NO3-)∶c(NO2-)=1∶9,则原混合气体中NO2和NO的物质的量之比n∶m=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 水的电离方程式:H2O = H++ OH-
B. pH=7的溶液一定是中性溶液
C. 升高温度,水的电离程度增大
D. 将稀醋酸加水稀释时,c(H+)减小,c(OH-)也减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com