
| A、稳定性:HF、H2O、PH3 |
| B、碱性:Al(OH)3、Mg(OH)2、NaOH |
| C、酸性:H2CO3、HClO4、H2SO4 |
| D、与氢气反应的难易程度:Br2、Cl2、F2 |


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
| A、服用铬含量超标的药用胶囊会对人对健康造成危害 |
| B、食用一定量的油脂能促进人体对某些维生素的吸收 |
| C、明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| D、镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
12 6 |
13 6 |
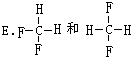
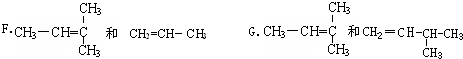
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管A中,滴加2mol?L-1 HCl至溶液呈酸性,加入几滴 | |
| 步骤② | 另取少量待测液于试管B中,加入 1mol?L-1 BaCl2溶液 | |
| 步骤③ | 另取少量待测液于试管C中, | 溶液分层,上层液体呈橙红色,证明待测液中很Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鸡蛋清溶液中加入饱和硫酸铵溶液,生成白色沉淀 |
| B、往Fe(OH)3胶体中逐滴加入稀硫酸会先产生沉淀而后沉淀逐渐溶解 |
| C、水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘粒子带电荷 |
| D、纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、结合质子(H+)能力:OH->CH3COO->Cl- |
| B、除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| C、F、Cl、Br的最外层电子数都是7,次外层电子数都是8 |
| D、X、Y均为短周期元素,其简单离子mXa+与nYb-的电子层结构相同,则m+a=n-b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中所有生成物都属于电解质 |
| B、反应中氧化剂与还原剂物质的量之比为1:6 |
| C、该反应表明氧化性KClO3比Cl2强 |
| D、生成6.72L的氯气,转移电子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①④⑥ |
| C、①②⑥ | D、②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com