
����Ŀ��ͭ����������;�㷺�Ľ�������ҵ�����õ�����ࣨ��Ҫ����Fe2O3��CuO��Cr2O3�������������ʣ����ս���ͭ����������ͼ�ף���֪���������ʳ�����pH�����
Fe3+ | Cu2+ | Cr3+ | |
��ʼ����pH | 2.1 | 4.7 | 4.3 |
��ȫ����pH | 3.2 | 6.7 | a |

CaSO4���ܽ��������ͼ�ң���ش��������⣺
��1����ҺI������������Ҫ�����ѧʽ����
��2���ڢڲ������У��ȼ���Ca��OH��2������Һ��pH�����ڷ�ΧΪ �� Ȼ����Һ������80����ȹ��ˣ�����������ijɷ�Ϊ ��
��3���ڢ۲������У����ֳ�������ש��ɫ�����⣬����������ɫ�̼�����ζ�����壮д���ò����з�����Ӧ�����ӷ���ʽ
��4��������Ũ�ȡ�1��10��5molL��1lʱ��������Ϊ���ӳ�����ȫ���ڢܲ������У���ҪʹCr3+��ȫ����������������Һ��a����СֵΪ �� ����֪Kap[Cr��OH��3]=6.3��10��31 �� ![]() ��4.0��lg4=0.6��
��4.0��lg4=0.6��
��5��Cr��OH��3���ȷֽ�ΪCr2O3 �� �����ȷ�����ұ����������д�����ȷ������Ļ�ѧ����ʽ ��
���𰸡�
��1��Fe2��SO4��3��Cr2��SO4��3��CuSO4
��2��3.2��pH��4.3��Fe��OH��3��CaSO4
��3��2H2O+HSO3��+2Cu2+=Cu2O��+SO42��+5H+��HSO3��+H+=SO2��+H2O
��4��5.6
��5��Cr2O3+2Al ![]() Al2O3+2Cr
Al2O3+2Cr
���������⣺�������м���ϡ���ᣬ������ӦFe2O3+3H2SO4=Fe2��SO4��3+3H2O��CuO+H2SO4=CuSO4+H2O��Cr2O3+3H2SO4=Cr2��SO4��3+3H2O��Ȼ����˵õ�����I����ҺI����ҺI������ΪFe2��SO4��3��Cr2��SO4��3��CuSO4 �� ����Һ�м���Ca��OH��2 �� ��������ҺpH����������ͼ����ҺII�к���Cr3+��Cu2+ �� ����Fe3+ �� ˵������II�к���Fe��OH��3 �� ���������������Գ���II�ɷ�ΪFe��OH��3��CaSO4 �� ҪʹCr3+��Cu2+��������Fe3+���������������������ɳ�����ҪpHֵ֪����Һ��pH��ΧΪ3.2��4.3֮�䣻����Һ�м���NaHSO3 �� ���������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3��+2Cu2+=Cu2O��+SO42��+5H+��HSO3��+H+=SO2��+H2O�����˵õ�Cu2O������Һ�м���NaOH��������ҺpH��������ӦCr3++3OH��=Cr��OH��3������ҺIV�к���NaOH��Na2SO4 �� ��1��ͨ�����Ϸ���֪����ҺI�����ʳɷ�ΪFe2��SO4��3��Cr2��SO4��3��CuSO4 �� ���Դ��ǣ�Fe2��SO4��3��Cr2��SO4��3��CuSO4����2��Fe3+��ȫ������Ҫ��pH��3.2��pH=4.3ʱCr3+��ʼ����������Ҫʹ��������ȫ�������������Ӳ���������pH��ΧΪ��3.2��pH��4.3��ͨ�����Ϸ���֪������II�ɷ�ΪFe��OH��3��CaSO4 �� ���Դ��ǣ�3.2��pH��4.3�� Fe��OH��3��CaSO4����3�����������ƾ��л�ԭ�ԡ�ͭ���Ӿ��������ԣ����߷���������ԭ��Ӧ���������ש��ɫ����Cu2O�������������������ӷ�Ӧ���ɶ����������ӷ���ʽΪ2H2O+HSO3��+2Cu2+=Cu2O��+SO42��+5H+��HSO3��+H+=SO2��+H2O�����Դ��ǣ�2H2O+HSO3��+2Cu2+=Cu2O��+SO42��+5H+��HSO3��+H+=SO2��+H2O����4��������Ũ�ȡ�1��10��5molL��1ʱ��������Ϊ���ӳ�����ȫ����ҪʹCr3+��ȫ��������c��Cr3+����1��10��5molL��1 �� c��OH����= ![]() =
= ![]() mol/L=4.0��10��9 mol/L��c��H+��=
mol/L=4.0��10��9 mol/L��c��H+��= ![]() =2.5��10��6mol/L������Һ��pH=��lg2.5��10��6=5.6��
=2.5��10��6mol/L������Һ��pH=��lg2.5��10��6=5.6��
���Դ��ǣ�5.6����5��Cr2O3��Al�����·������ȷ�Ӧ������������Cr����Ӧ����ʽΪCr2O3+2Al ![]() Al2O3+2Cr�����Դ��ǣ�Cr2O3+2Al
Al2O3+2Cr�����Դ��ǣ�Cr2O3+2Al ![]() Al2O3+2Cr��
Al2O3+2Cr��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о���ѧϰС�����һ�����ԭ�ϣ������ֶ����ڵij�����������Li��Na��Mg��Al��ɵĺϽ��ĩ������̽�������������̽�����森
��̽��Ŀ�ġ�̽�������ԭ�ϵ����
�����ϼ�������Mg2+���鷽����ȡ2�δ���Һ������2��2molL��1NaOH��Һ���ټ���1��þ�Լ�����Ⱦ�ϣ���������ż�������ӣ��������ֳ���������þ�Լ�����Ⱦ�ϳ�����ɫ����ʾ����Һ�к���Mg2+ �� ��Ag+��Cu2+��Fe3+��NH4+�����Mg2+���
��Mg��OH��2������Ũ���Ȼ����Һ�������ij������ܼ��������Ȼ��
�ۺܶ�Ͻ��ǽ����������ȷ���Ļ�ѧ���
��̽��˼·����ȷ�����ԭ�������������ࣻ�ڲⶨ���ԭ�ϵĻ�ѧʽ
��ʵ��̽����
��1����ͬѧ�����˳������飬ʵ�鲽���ʵ���������£�����д�±���
������� | ʵ �� �� �� | ʵ �� �� �� | �� �� |
�� | ȡ���������ԭ�ϼ�����ˮ | ���������� | |
�� | ȡ���������ԭ�ϼ���ϡ���� | ��ȫ�ܽ⣬�д��������������Һ����ɫ |
��2����ͬѧȡ�ڢ���ʵ�����Һ������þ�Լ�����Ⱦ�ϣ��ó��Ͻ��в���þ���ҵĽ�����ѡ���ȷ����������������� ��
��3����ͬѧ���ʵ�鷽����ȷ�����ԭ���еĽ������࣬ʵ���¼���£�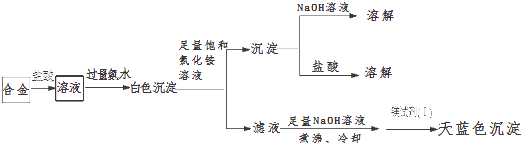
�ɱ���ʵ���¼��֪�������ԭ�����������ֽ�����ɵĺϽ�ʵ������Һ������������������Һ������У���е������� ��
��4����ͬѧ���ñ�ͬѧ�Ľ��ۣ��������ͼ��ʾ��ʵ�鲽�裬ȷ���Ͻ���ɣ�
�������ۣ�
����ȷ���Ͻ���ɵ�������������дѡ����ĸ����
A��m��n B��m��y C��n��y
�����Ͻ������ԭ��������С�Ľ��������ʵ�������Ϊx�����������ʵ���Ϊ7mol��������ͼ������y��x�仯������ ��
�۵�y=8.5molʱ���úϽ���һ�ֽ���������仯ѧʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����м׳ص��ܷ�ӦΪ��2CH3OH+3O2+4KOH=2K2CO3+6H2O����˵����ȷ���ǣ� �� 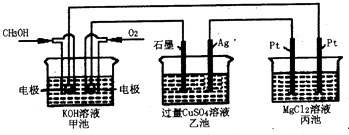
A.�׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҡ������ǻ�ѧ��ת�����ܵ�װ��
B.�׳�ͨ��CH3OH�ĵ缫��ӦΪCH3OH��6e��+2H2O=CO32��+8H+
C.��Ӧһ��ʱ������ҳ��м���һ����Cu��OH��2���壬��ʹCuSO4��Һ�ָ���ԭŨ��
D.�׳�������560mL����״���£�O2 �� ��ʱ������������������2.9g����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ӦI��4NH3��g��+6NO��g��5N2��g��+6H2O��l����H1��Ӧ��2NO��g��+O2��g��2NO2��g����H2����|��H1|=2|��H2|��
��Ӧ��4NH3��g��+6NO2��g��5N2��g��+3O2��g��+6H2O��l����H 3
��ӦI�ͷ�Ӧ���ڲ�ͬ�¶�ʱ��ƽ�ⳣ�������С��ϵ���±�
�¶�/K | ��ӦI | ��ӦII | ��֪�� |
298 | K1 | K2 | |
398 | K1�� | K2�� |
��1����H3=���á�H1����H2�Ĵ���ʽ��ʾ�����ƲⷴӦ������Ӧ������ȡ����ȡ���
��2����ͬ�����£���ӦI��4NH3��g��+6NO��g��5N2��g��+6H2O��l����2L�ܱ������ڣ�ѡ�ò�ͬ�Ĵ�������Ӧ����N2������ʱ��仯��ͼ��ʾ�� �ټ���0��4������A���������£���Ӧ����V��NO��= ��
������˵������ȷ���� ��
A����λʱ����H��O����N��H�����ѵ���Ŀ���ʱ��˵����Ӧ�Ѿ��ﵽƽ��
B�����ں��ݾ��ȵ��ܱ������з�����Ӧ����Kֵ����ʱ��˵����Ӧ�Ѿ��ﵽƽ��
C���÷�Ӧ�Ļ�ܴ�С˳���ǣ�Ea��A����Ea��B����Ea��C��
D������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ�����˻���Ӱٷ���
��3��һ�������£���ӦII�ﵽƽ��ʱ��ϵ��n��NO����n��O2����n��NO2��=2��1��2�� �ٱ��ֺ��º��ݣ��ٳ���NO2���壬NO2�����������������С�����䡱��
�ڹ���ƽ����ϵ��Ӧ��2NO��g��+O2��g��2NO2��g������H2˵����ȷ���� ��
A���÷�Ӧ�ʱ�Ϊ��ֵ
B�������¶ȣ��淴Ӧ������������Ӧ���ʼ�С����Ӧ�����ƶ�
C����������ѹǿ���Ǽ�Сѹǿ�����������ʸı�ij̶ȸ���
D��ƽ�������ƶ���NO��ת����һ������
E��ƽ����ϵ�м���NO2 �� ƽ�������ƶ�����H2��С
F�����������ɫ����˵��ƽ�������ƶ�����ɫ��dz�������ƶ���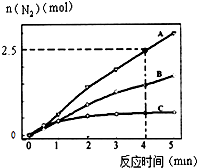
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ӦI��4NH3��g��+6NO��g��5N2��g��+6H2O��l����H1��Ӧ��2NO��g��+O2��g��2NO2��g����H2����|��H1|=2|��H2|��
��Ӧ��4NH3��g��+6NO2��g��5N2��g��+3O2��g��+6H2O��l����H 3
��ӦI�ͷ�Ӧ���ڲ�ͬ�¶�ʱ��ƽ�ⳣ�������С��ϵ���±�
�¶�/K | ��ӦI | ��ӦII | ��֪�� |
298 | K1 | K2 | |
398 | K1�� | K2�� |
��1����H3=���á�H1����H2�Ĵ���ʽ��ʾ�����ƲⷴӦ������Ӧ������ȡ����ȡ���
��2����ͬ�����£���ӦI��4NH3��g��+6NO��g��5N2��g��+6H2O��l����2L�ܱ������ڣ�ѡ�ò�ͬ�Ĵ�������Ӧ����N2������ʱ��仯��ͼ��ʾ�� �ټ���0��4������A���������£���Ӧ����V��NO��= ��
������˵������ȷ���� ��
A����λʱ����H��O����N��H�����ѵ���Ŀ���ʱ��˵����Ӧ�Ѿ��ﵽƽ��
B�����ں��ݾ��ȵ��ܱ������з�����Ӧ����Kֵ����ʱ��˵����Ӧ�Ѿ��ﵽƽ��
C���÷�Ӧ�Ļ�ܴ�С˳���ǣ�Ea��A����Ea��B����Ea��C��
D������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ�����˻���Ӱٷ���
��3��һ�������£���ӦII�ﵽƽ��ʱ��ϵ��n��NO����n��O2����n��NO2��=2��1��2�� �ٱ��ֺ��º��ݣ��ٳ���NO2���壬NO2�����������������С�����䡱��
�ڹ���ƽ����ϵ��Ӧ��2NO��g��+O2��g��2NO2��g������H2˵����ȷ���� ��
A���÷�Ӧ�ʱ�Ϊ��ֵ
B�������¶ȣ��淴Ӧ������������Ӧ���ʼ�С����Ӧ�����ƶ�
C����������ѹǿ���Ǽ�Сѹǿ�����������ʸı�ij̶ȸ���
D��ƽ�������ƶ���NO��ת����һ������
E��ƽ����ϵ�м���NO2 �� ƽ�������ƶ�����H2��С
F�����������ɫ����˵��ƽ�������ƶ�����ɫ��dz�������ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ��������(����ͼ��ʾ)������������ơ���֪����1molN-N������193kJ����������1molN��N������941kJ������������˵������ȷ����

A. N4��N2��Ϊͬ��������
B. 1molN4����ת��ΪN2ʱҪ����724kJ����
C. N4���N2�ǻ�ѧ�仯
D. N4��������6�����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijģ�⡰�˹���Ҷ���绯ѧʵ��װ������ͼ��ʾ����װ���ܽ�H2O��CO2ת��ΪO2��ȼ��(C3H8O)������˵����ȷ����

A. a�缫�ķ�ӦΪ: 3CO2 + 18H��-18e��= C3H8O+5H2O
B. ��װ�ý���ѧ��ת��Ϊ���ܺ͵���
C. ��װ�ù���ʱH+��b������a����Ǩ��
D. ÿ����1molO2����44gCO2����ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ���ۺϴ���SO2�����Ĺ������̡�����˵����ȷ����(����)
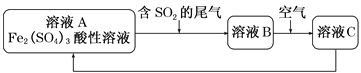
A. ����ҺB�еμ�KSCN��Һ����Һһ��������ɫ
B. ��ҺAת��Ϊ��ҺB������Ӧ�����ӷ���ʽΪ��2Fe3����2H2O��SO2===2Fe2����SO![]() ��4H��
��4H��
C. ��Һ���ԣ�B>C>A
D. ��������������ʹ��ҺCת��Ϊ��ҺA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A. �����ЧӦ���ǽ������е�������Һ����ҺҲ��
B. ������������ɢϵ�ı����������ж����ЧӦ����������ɢϵû��
C. �������ӵ�ֱ��С��10��9m
D. �����ЧӦ�����ڼ��������Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com