

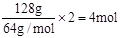 所以根据电子得失守恒可知,消耗氧气是1mol,则空气是5mol,标准状况下的体积是5mol×22.4L/mol=112L。
所以根据电子得失守恒可知,消耗氧气是1mol,则空气是5mol,标准状况下的体积是5mol×22.4L/mol=112L。

 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源:不详 题型:填空题
 2NO (g),该反应是导致汽车尾气中含有NO的原因之一。
2NO (g),该反应是导致汽车尾气中含有NO的原因之一。
 N2(g)+O2(g)。反应过程中N2的体积分数随时间变化的图像。升高温度,则反应N2 (g)+O2(g)
N2(g)+O2(g)。反应过程中N2的体积分数随时间变化的图像。升高温度,则反应N2 (g)+O2(g) 2NO (g)的平衡常数K将 (填“增大”、“减小”或“不变”)。
2NO (g)的平衡常数K将 (填“增大”、“减小”或“不变”)。 2NO (g)的平衡常数K的数值为 。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为 。
2NO (g)的平衡常数K的数值为 。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2H+(aq) +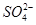 (aq)+ (aq)+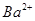 (aq)+2 (aq)+2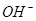 (aq) = BaSO4(s)+2H (aq) = BaSO4(s)+2H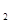 O(l); O(l);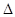 H = H =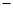 57.3 kJ/mol 57.3 kJ/mol |
B.KOH(aq)+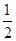 H H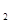 SO4(aq) = SO4(aq) = 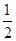 K K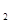 SO4(aq)+H SO4(aq)+H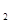 O(l); O(l);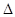 H= H=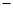 57.3kJ/mol 57.3kJ/mol |
C.C8H18(l)+ 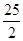 O O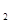 (g)=8CO (g)=8CO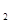 (g)+ 9H (g)+ 9H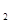 O(g); O(g);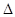 H= H=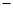 5518 kJ/mol 5518 kJ/mol |
D.2C8H18(g)+25O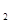 (g)=16CO (g)=16CO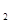 (g)+18H (g)+18H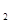 O(1); O(1);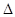 H= H=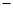 5518 kJ/mol 5518 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学键 | H—H | Cl—Cl | H—Cl |
| 键能/kJ·mol-1 | 436 | 243 | 431 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
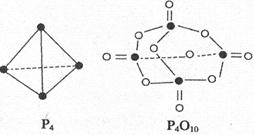
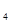 +5O
+5O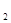 =P
=P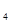 O
O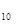 。已知断裂下列化学键需要吸收的能量分别为:P-Pa kJ·mol
。已知断裂下列化学键需要吸收的能量分别为:P-Pa kJ·mol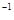 、P-O b kJ·mol
、P-O b kJ·mol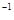 、P="=O" c kJ·mol
、P="=O" c kJ·mol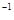 、O="=O" d kJ·mol
、O="=O" d kJ·mol
A.(6a+5d-4c-12b) kJ·mol | B.(4c+12b-6a-5d) kJ·mol |
C.(4c+12b-4a-5d) kJ·mol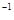 | D.(4a+5d-4c-12b) kJ·mol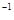 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1 CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1
CH3CH2OH(g)+3H2O(g) △H =" —173.6" kJ·mol-1 2CH3OH的热化学方程式为:__________________。
2CH3OH的热化学方程式为:__________________。

 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4Q1+0.5Q2 | B.4Q1+Q2+10Q3 | C.4Q1+2Q2 | D.4Q1+0.5Q2+9Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g) + H2(g) △H1=" +" 41.2kJ/mol
CO2(g) + H2(g) △H1=" +" 41.2kJ/mol CO2(g) + H2(g) △H1=" +" 41.2kJ/mol
CO2(g) + H2(g) △H1=" +" 41.2kJ/mol查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-69.4kJ/mol | B.-45.2 kJ/mol | C.+69.4kJ/mol | D.+45.2 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com