
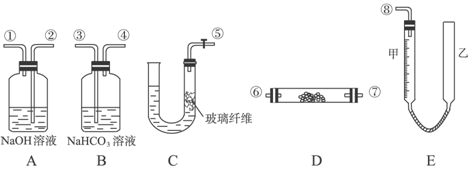
分析 题目要求利用过氧化钠与二氧化碳(潮湿)反应制取氧气,故首先需要制备二氧化碳.只有仪器C可以用来制取二氧化碳.制气原料应该采用大理石和盐酸,此法制得的二氧化碳中会含有少量氯化氢.须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢.然后使净化后的二氧化碳通过过氧化钠来制取氧气,该仪器只能选用装置D.此反应属于气体与固体之间的反应,不易反应完全,为了除去生成的氧气中混有未反应的二氧化碳,可以使它们通过仪器A.在测量氧气体积时,为了使测量更为准确,要注意上下移动仪器E中的乙管,使甲、乙两管的液面相平,以使甲管中的气压与大气气压相等,同时视线应与甲管内凹液面最低处相平,以减少观察误差,
(1)仪器C可以用来制取二氧化碳,连接3用来除去HCl,4连接6可使二氧化碳与过氧化钠反应生成氧气,然后连接2可除去未反应的二氧化碳,最后连接8测量气体的体积,据此分析装置连接顺序;
(2)只有仪器C可以用来制取二氧化碳,制气原料应该采用大理石和盐酸;
(3)装置D中是二氧化碳、水蒸气通过过氧化钠来制取氧气:2Na2O2+2CO2=2Na2CO3+O2↑,故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;
(4)仪器C可以用来制取二氧化碳,此法制得的二氧化碳中会含有少量氯化氢,须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢,净化后的二氧化碳通过过氧化钠来制取氧气,通过氢氧化钠溶液吸收混在氧气中的二氧化碳气体;
(5)排水量器操作注意:①读数时要调节E中甲乙的液面使其同一高度;②读数时视线要与凹液面最低处相平,③恢复到室温;
(6)反应结束后,测得产生的气体标准状况下体积为22.4mL,为过氧化钠生成的氧气,2mol过氧化钠反应生成1mol氧气,电子转移2mol.
解答 解:(1)仪器C可以用来制取二氧化碳,连接3用来除去HCl,4连接6可使二氧化碳与过氧化钠反应生成氧气,然后连接2可除去未反应的二氧化碳,最后连接8测量气体的体积,所以顺序为:⑤③④⑥⑦②①⑧(⑥、⑦可换位),
故答案为:⑤③④⑥⑦②①⑧(⑥、⑦可换位);
(2)只有仪器C可以用来制取二氧化碳,制气原料应该采用大理石和盐酸,可在C中加止水夹,可控制反应的进行,
故答案为:大理石;盐酸;
(3)装置D中是二氧化碳、水蒸气通过过氧化钠来制取氧气,反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑2Na2O2+2CO2=2Na2CO3+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;2Na2O2+2CO2=2Na2CO3+O2↑;
(4)仪器C可以用来制取二氧化碳,此法制得的二氧化碳中会含有少量氯化氢,须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢,净化后的二氧化碳通过过氧化钠来制取氧气,为了除去生成的氧气中混有未反应的二氧化碳,可以使它们通过仪器A,
故答案为:除去混在O2中未反应的CO2;吸收CO2中混有的HCl;
(5)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数.求其差值的过程中,应注意:①读数时要调节E中甲乙的液面使其同一高度;②读数时视线要与凹液面最低处相平,故答案为:a、c.
(6)反应结束后,测得产生的气体标准状况下体积为22.4mL,为过氧化钠生成的氧气物质的量=$\frac{0.0224L}{22.4L/mol}$=0.001mol,2mol过氧化钠反应生成1mol氧气,电子转移2mol,电子转移物质的量0.002mol,转移的电子数目为6.02×1023×0.002mol×NA=1.204×1021,
故答案为:1.204×1021.
点评 本题考查过氧化钠与二氧化碳的反应,并考查气体的制备、除杂、量气等知识,题目难度中等,本题注意把握实验原理和操作方法,注重基础知识的积累.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一有机反应类型 | |
| B. | 单质硅是将太阳能转化为电能的常用材料 | |
| C. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
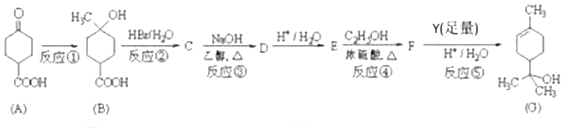
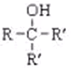
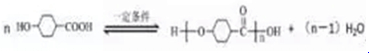 .写出同时满足下列条件的B的同分异构体的结构简式
.写出同时满足下列条件的B的同分异构体的结构简式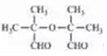 .
.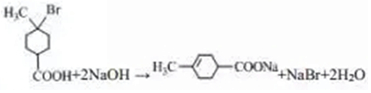 ,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为
,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为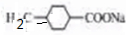 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com