
【题目】25℃,有两种盐的稀溶液,分别是![]() mol/L NaX溶液和
mol/L NaX溶液和![]() mol/L NaY溶液,下列判断错误的是( )
mol/L NaY溶液,下列判断错误的是( )
A. 若![]() ,测得
,测得![]() ,则溶液中的
,则溶液中的![]()
B. 若![]() ,测得
,测得![]() ,则溶液中的
,则溶液中的![]()
C. 若![]() ,且
,且![]() ,则酸性:
,则酸性: ![]()
D. 若![]() ,并测得
,并测得![]() ,则HX是强酸,HY是弱酸
,则HX是强酸,HY是弱酸
【答案】B
【解析】A、NaX的浓度大于NaY的浓度,但X-的浓度等于Y-的浓度,说明NaX水解,NaY不水解或是NaX水解程度大于NaY,酸越弱,越水解,所以酸性HX<HY,溶液中的c(HX)>c(HY),故A正确。B、NaX的浓度大于NaY的浓度,且HX的浓度大于HY的浓度,说明X-水解程度大,Y-水解程度小,酸越弱,越水解,所以原溶液中X-应大于Y-的浓度,故B错误。C、根据酸越弱,越水解可以知道,若a=b,则pH(NaX)>pH(NaY),则酸性:HX<HY,故C正确。D、若a=b且a=c(X-)=c(Y-)+c(HY),则HX是强酸,HY是弱酸,酸性HX>HY,故D正确。本题的正确选项为B。;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
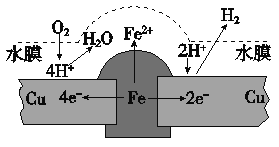
A. 因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B. 若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C. 铜极上的反应是2H+ + 2e- = H2↑,O2 + 4e-+ 4H+ = 2H2O
D. 在金属表面涂一层油脂,能防止铁铆钉被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X和Y两元素组成化合物A和B,A的化学式为XY2,其中X占44.1%,B中X占34.5%,则B的化学式为( )
A.X2YB.XYC.XY3D.X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高压电机,复印机工作时会产生臭氧,该气体有强氧化性。下列叙述不正确的是( )
A、臭氧和氧气互为同素异形体 B、臭氧可使KI淀粉试纸变蓝
C、臭氧的存在对人体有益无害 D、臭氧是很好的消毒剂和脱色剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.含有共价键的化合物一定是共价化合物
B.气态单质分子中一定存在共价键
C.含有离子键的化合物一定是离子化合物
D.含有离子键的化合物不一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的催化氧化: ![]() ,是工业制取硫酸的关键步骤之一。在容积都为2L的
,是工业制取硫酸的关键步骤之一。在容积都为2L的![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 五个密闭容器中,投入相同的催化剂,并均充入1mol O2和2mol SO2,控制不同的反应温度进行反应,反应进行到5min时,测得相关数据如下表:
五个密闭容器中,投入相同的催化剂,并均充入1mol O2和2mol SO2,控制不同的反应温度进行反应,反应进行到5min时,测得相关数据如下表:
容器温度 物质的量(mol) |
400℃ |
425℃ |
450℃ |
475℃ |
500℃ |
O2 | 0.8 | 0.6 | 0.3 | 0.5 | 0.7 |
SO3 | 0.4 | 0.8 | 1.4 | 1.0 | 0.6 |
(1)计算5min内![]() 容器中SO2的平均反应速率___________________________。
容器中SO2的平均反应速率___________________________。
(2)反应进行到5min时, ![]() 容器中的反应是否达到平衡状态?_______(填“已达”、“未达”)理由是:_________________________________________________
容器中的反应是否达到平衡状态?_______(填“已达”、“未达”)理由是:_________________________________________________
(3)在右图中画出![]() 容器中SO3物质的量随时间的变化曲线。____________
容器中SO3物质的量随时间的变化曲线。____________
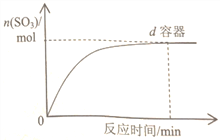
(4)工业上常用Na2SO3溶液来吸收SO2,该反应的离子方程式是:______________________。
(5)Na2SO3和NaHSO3混合溶液的pH随Na2SO3和NaHSO3比例的不同而不同,数据如下:
序号 | ① | ② | ③ |
| 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
表中第________组(填写序号)数据,可判断NaHSO3溶液显_______性(填“酸”或“碱”)。
(6)NaHSO3既能和强酸反应也能和强碱溶液反应。用平衡移动原理说明NaHSO3能和强碱溶液反应的原因:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是
A. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32 -)>c(HCO3- )>c(OH-)
B. CH3COOH溶液加水稀释,溶液中![]() 不变
不变
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D. 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融) ![]() 2Na+Cl2↑。已知A、B、C、D、E有如下转化关系:
2Na+Cl2↑。已知A、B、C、D、E有如下转化关系:
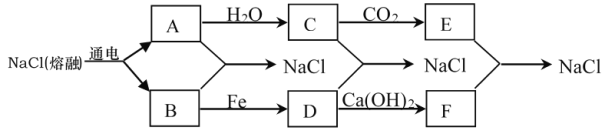
(1)写出A、B生成NaCl的化学方程式:_____________________________________。
(2)写出化学式:C______________,D_____________。
(3)工业生产中常利用B与Ca(OH)2反应来制备漂白粉,漂白粉的主要成分是_______________________________。(写化学式)
(4)若把A投入盛有D的溶液中,溶液中出现________________(填沉淀颜色)沉淀,该过程所发生反应的化学方程式为____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com