

| ||
| 80 |
| x |
| 18 |
| 1.8 |
| 64 |
| 64+16 |
| 10.0g-8.0g+6.4g |
| 10.0g |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
| A、Na+、Cl-、NO3- |
| B、Ag+、Cl-、NO3- |
| C、NH4+、OH-、SO42- |
| D、Na+、Fe2+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若金属有剩余,在溶液中再滴入硫酸后,金属不再溶解 | ||
| B、若金属全部溶解后,再加入KSCN溶液,则溶液一定呈血红色 | ||
| C、若金属全部溶解,且产生336 mL气体(标准状况),则b=0.3 | ||
D、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 配料表 | 精制海盐、碘酸钾 |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
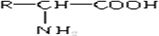 ,其分子中一定含有羧基(-COOH)和
,其分子中一定含有羧基(-COOH)和 是一种重要的合成材料,契单体的结构简式为
是一种重要的合成材料,契单体的结构简式为
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有甲、乙、丙、丁4种物质,其转化关系如图:
现有甲、乙、丙、丁4种物质,其转化关系如图:查看答案和解析>>
科目:高中化学 来源: 题型:
 )由两分子某链状有机物A反应得到,则与链状有机物A互为同分异构体且含有相同官能团的结构简式为
)由两分子某链状有机物A反应得到,则与链状有机物A互为同分异构体且含有相同官能团的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
A、HCO
| ||||
B、Al3+、K+、OH-、SO
| ||||
C、Fe3+、I-、SO
| ||||
D、K+、Al3+、SO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com